XI. Kinetische Gastheorie
Definition IIX.1: Ein Ideales Gas ist ein Gas, in dem die zwischenmolekularen Kräfte null sind und die Moleküle keine Ausdehnung haben (punktförmig sind). |
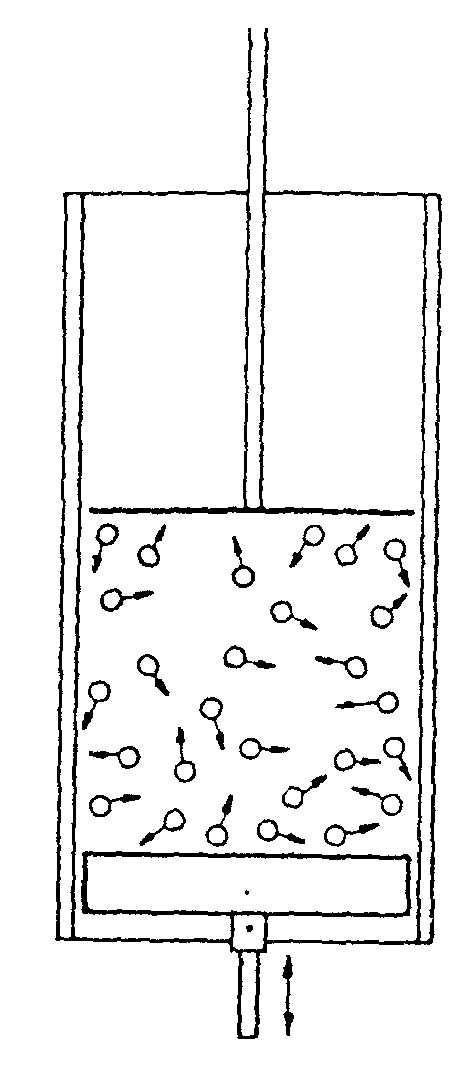 Wie wir bereits festgestellt hatten, kann man sich wie die idealen Gase in einem einfachen Modell veranschaulichen:
Als Modell eines idealen Gases kann man sich ein geschlossenes Volumen vorstellen, in dem elastische Kugeln ohne sich zu berühren regellose Bewegungen ausführen. Selbstverständlich sind die Kugeln nicht immer gleichmäßig über den Raum verteilt. Stellt man sich dem Druck nun so vor, daß die Kugeln an die Gefäßwand treffen, so folgt aus dieser ungleichen Verteilung eine statistische Schwankungen der Kraft, die ein eingesperrtes Gas auf einen Kolben ausübt. Dieses Phänomen wollen wir in diesem Kapitel untersuchen.
Wir hatten ideale Gase definiert als Gase, bei denen keine Bindungskräfte zwischen den einzelnen Molekülen existieren. Es gibt einige Gase, die diesem Kriterium nahezu gerecht werden. Physikalischen kann man ideale Gase auch in anderen Fällen realisieren, indem man das Gas hinreichend verdünnt. Die Anziehungskräfte zwischen den einzelnen Molekülen werden dann beliebig klein.
Dieser Idealisierung entspricht der Idealisierung des Massepunktes in der Mechanik. Tatsächlich wollen wir versuchen, das Verhalten der idealen Gase auf mechanische Gesetze zurückzuführen, indem wir die Moleküle als bewegte Massepunkte auffassen.
Wie wir bereits festgestellt hatten, kann man sich wie die idealen Gase in einem einfachen Modell veranschaulichen:
Als Modell eines idealen Gases kann man sich ein geschlossenes Volumen vorstellen, in dem elastische Kugeln ohne sich zu berühren regellose Bewegungen ausführen. Selbstverständlich sind die Kugeln nicht immer gleichmäßig über den Raum verteilt. Stellt man sich dem Druck nun so vor, daß die Kugeln an die Gefäßwand treffen, so folgt aus dieser ungleichen Verteilung eine statistische Schwankungen der Kraft, die ein eingesperrtes Gas auf einen Kolben ausübt. Dieses Phänomen wollen wir in diesem Kapitel untersuchen.
Wir hatten ideale Gase definiert als Gase, bei denen keine Bindungskräfte zwischen den einzelnen Molekülen existieren. Es gibt einige Gase, die diesem Kriterium nahezu gerecht werden. Physikalischen kann man ideale Gase auch in anderen Fällen realisieren, indem man das Gas hinreichend verdünnt. Die Anziehungskräfte zwischen den einzelnen Molekülen werden dann beliebig klein.
Dieser Idealisierung entspricht der Idealisierung des Massepunktes in der Mechanik. Tatsächlich wollen wir versuchen, das Verhalten der idealen Gase auf mechanische Gesetze zurückzuführen, indem wir die Moleküle als bewegte Massepunkte auffassen.