X.3 Aggregatzustände
1. der Übergang vom festen zum flüssigen Körper und umgekehrt:
Wie wir bereits bei der Betrachtung der Reproduzierbarkeit eines Fixpunkts, der Temperatur, bei der Wasser und Eis koexistieren, voraus gesetzt hatten, tritt das Schmelzen bei kristallinen Stoffen stets bei der gleichen Temperatur ein Diese Temperatur ist eine Materialkonstante und heißt Schmelztemperatur oder Schmelzpunkt.
Führt man bei der Schmelztemperatur dem Körper durch Arbeit oder Wärme Energie zu, während der Druck konstant gehalten wird, so wird diese Energie zur Auflösung des Kristallgitters verwendet. Erst wenn der ganze Körper geschmolzen ist, erhöht sich bei weiterer Energiezufuhr die Temperatur der Flüssigkeit.
Entzieht man der Flüssigkeit hingegen die Energie, so erstarrt sie bei der Schmelztemperatur wieder.
2. den Übergang vom flüssigen zum gasförmigen Aggregatzustand:
Führt man bei der Siedetemperatur einer Flüssigkeit Energie bei konstantem Druck zu, so wird dieser dazu verwendet, die Moleküle aus dem Flüssigkeitsverband zu lösen. Das Volumen des Dampfes gegenüber der Flüssigkeit wird stark vergrößert. Erst wenn die ganze Flüssigkeit verdampft ist, erhöht sich bei weiterer Energiezufuhr die Temperatur des Dampfes. Der Entzug von Energie hat zur Folge, daß der Dampf kondensiert.
Die Abhängigkeit der Temperatur eines Körpers von der zugeführten Wärme läßt sich für verschiedene Körper messen. Aufgetragen in einem Q/T-Diagramm sieht man die Graden, also die konstanten Temperaturen, bei denen die zugeführte Energie keine Temperaturerhöhung sondern eine Änderung des Aggregatzustandes bewirkt. Diese Diagramme lassen sich für verschiedene Stoffe aufnehmen. Bei dem Diagramm für Eis-Wasser-Dampf können die Fixpunkte der Celsius-Skala abgelesen werden.
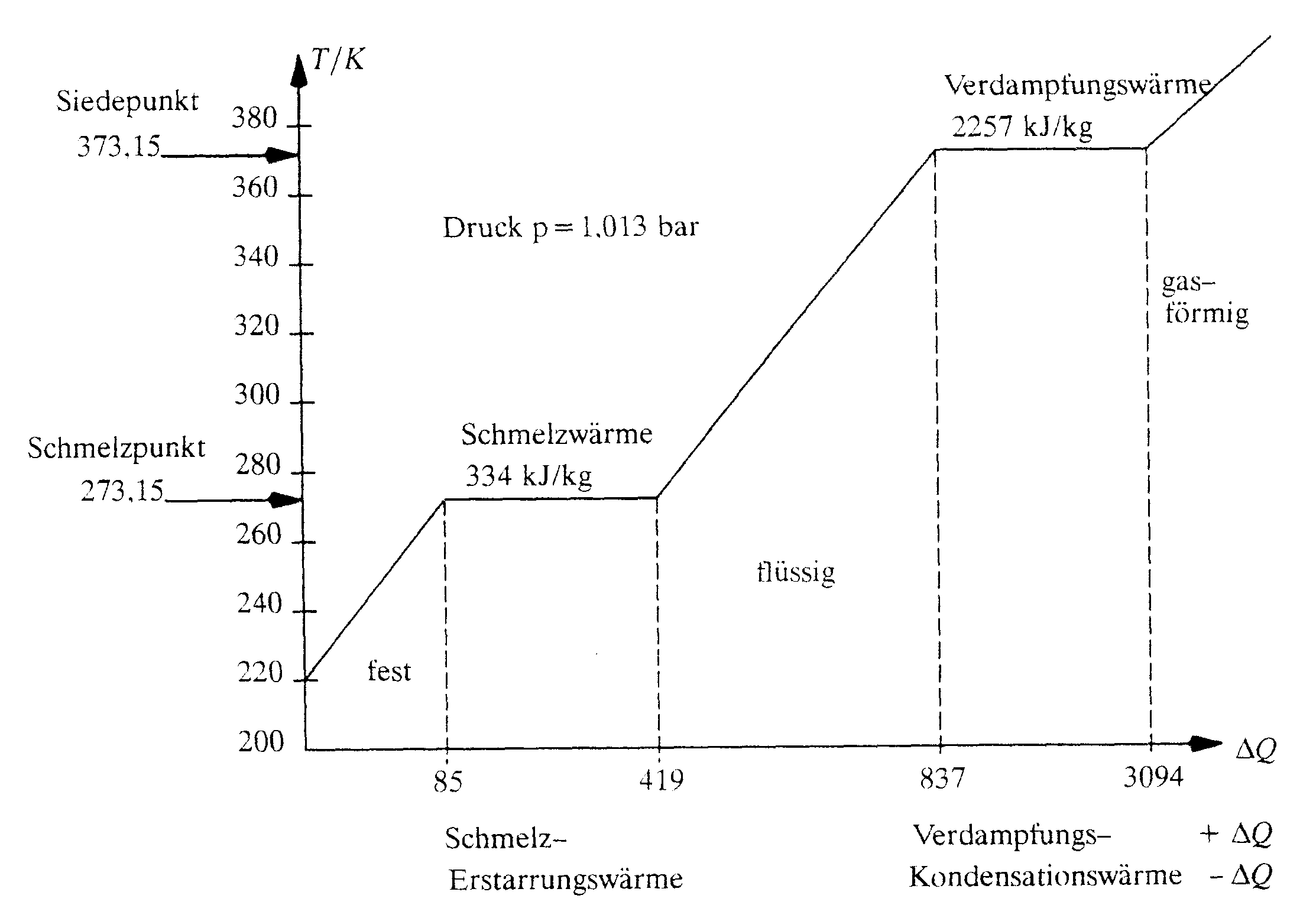
Aus diesen Diagrammen läßt sich der Zusammenhang von Druck p und Temperatur T mit den Grenzen zwischen den Aggregatzuständen konstruieren. Dabei tritt noch ein Übergang zwischen den Phasen auf:
3. Übergang vom Festkörper zum Gas
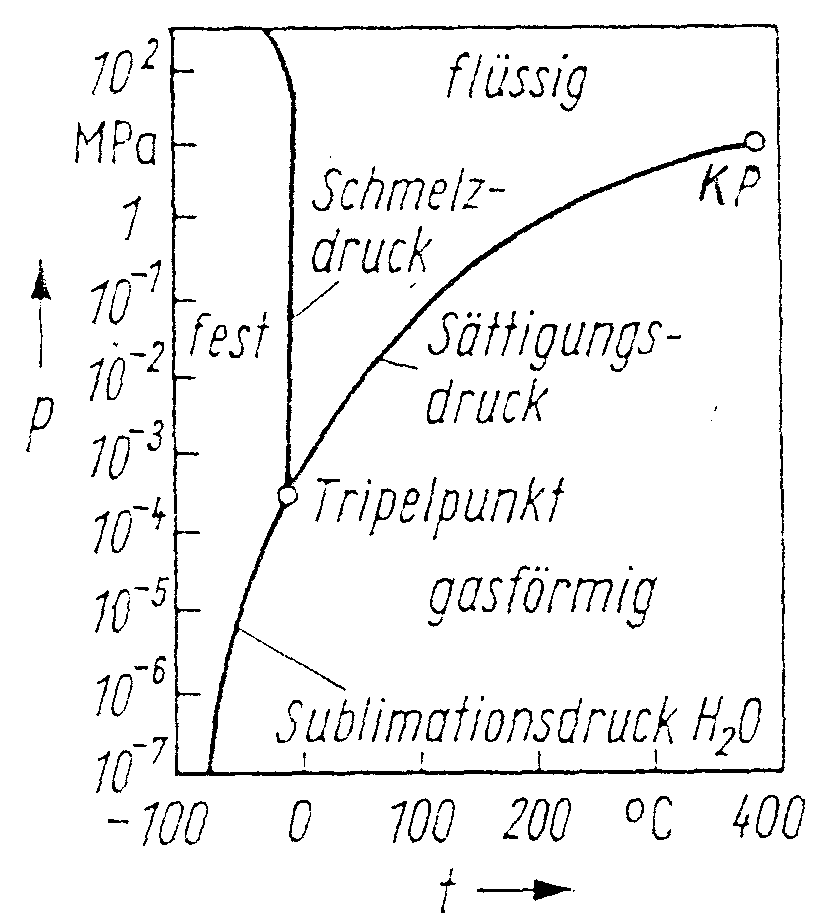
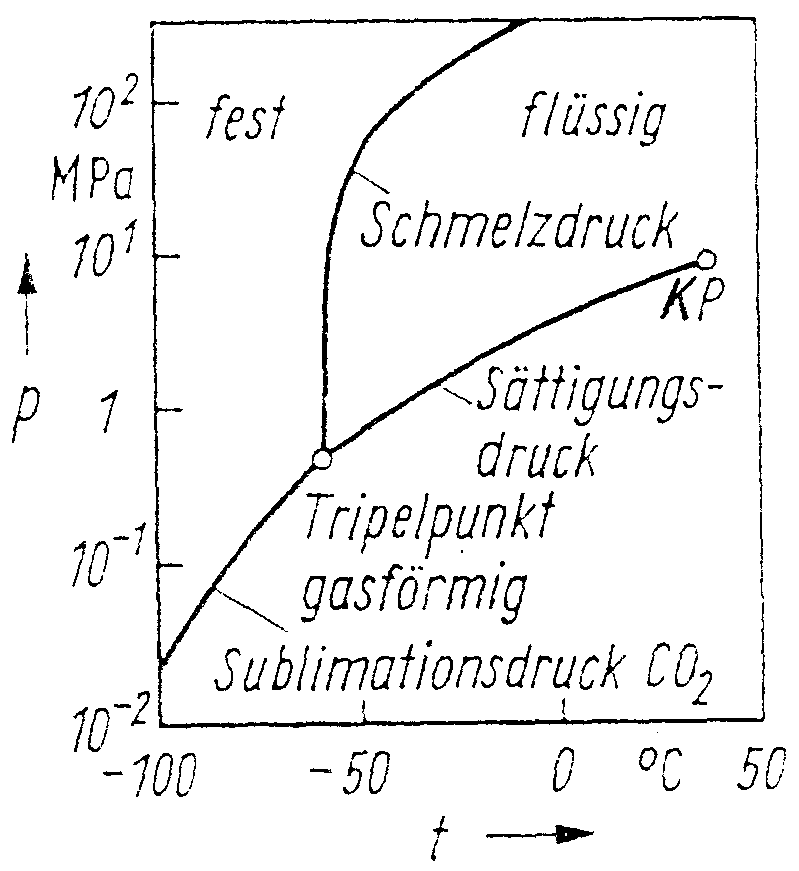
Im p,T Diagramm hat die Dampfdruckkurve ein viel geringere Steigung als die Schmelzkurve: Die beiden müssen sich also irgendwo treffen. Dieser Punkt wird Trippelpunkt genannt. An dieser Stelle können gasförmige, flüssige und feste Körper nebeneinander bestehen. Unterhalb und links dieses Punktes gibt es keinen flüssigen Zustand.
Merke: Nur im Trippelpunkt existieren alle drei Aggregatzustände gleichzeitig. |
Der Trippelpunkt liegt für H2O bei einem Druck von 6,1 mbar und 0,0075°C und für CO2 bei 5,1 mbar und -56°C.


Die Betrachtung dieser Zustandsdiagrammen zeigt, daß es noch einen weiteren, wichtigen Punkt gibt: den kritischen Punkt. Steigt die Temperatur über die kritische Temperatur tk, so kann der Stoff trotz Druckveränderung nicht mehr verflüssigt werden. Unterhalb der Temperatur tk kann mittels Druckerhöhung immer der Übergang in die flüssige Phase erzwungen werden. Oberhalb aber ist die Dichte des 'Gases' so groß, daß man nicht sagen kann, ob der Stoff gasförmig oder flüssig ist.
Merke: Oberhalb der kritischen Temperatur kann ein Stoff auch mit beliebiger Druckerhöhung nicht verflüssigt werden. |
Zu den Phasenübergängen wollen wir nun einen Versuch betrachten:
Versuch X.1: Kritischer Punkt
Bei diesem Versuchsaufbau ist in einem abgeschlossenen Zylinder zur Hälfte Freon 115 eingeschlossen bei einem festen Druck von 30,8 bar. Über ein Wasserbad, welches mit einem Tauchsieder erhitzt wird, kann die Temperatur dieses Stoffes variiert werden. Der Zylinder besteht teilweise aus Glas und wird mit einer Lampe durchleuchtet, so daß man die Vorgänge im Inneren betrachten kann.Zunächst ist die Temperatur des Wasserbades (und damit der Freon 155) unter 80°C. Man beobachtet unten im Zylinder eine Flüssigkeit und oberhalb Gas. Die Phasen sind klar exakt in der Mitte des Zylinders getrennt. Nun wird der Stoff erhitzt. Ab einer Temperatur von knapp 80°C steigt die flüssige Phase an und füllt immer mehr Raum aus. Ab der kritischen Temperatur von 80°C kann nur noch eine homogene Substanz beobachtet werden, die den ganzen Zylinder ausfüllt. Man kann nicht sagen, ob dieser Stoff flüssig oder gasförmig ist. Senkt man die Temperatur wieder, so bilden sich erneut zwei Phasen aus.