XI.2 Kinetische Gastheorie
Diese Überlegungen führten 1857 dazu, daß der deutsche Physiker Rudolf Clausius (1822 - 1888) den Zusammenhang zwischen der Mechanik und der Wärmelehre aufdeckte. Mit dem Versuch, die Idealgasgesetze aus dem mikroskopischen Verhalten der Moleküle zu verstehen, die im Sinne der Mechanik Massepunkt darstellen, begründete Clausius die kinetische Gastheorie.
Dabei gehen wir wieder auf das inzwischen vertraut gewordene Modell eines idealen Gases zurück, bei dem die Moleküle sich wie elastische Kugeln ohne Ausdehnung verhalten. Mit diesen beiden Annahmen:
1. die Moleküle sind Punktmassen
2. sie führen nur elastische Stöße aus
kann man überlegen, was im Inneren eines mit Gas gefüllten Gefäßes passiert. Dabei kann man zunächst berechnen, wie eine Punktmasse sich bewegt. Danach wird es jedoch schwierig, jede einzelne Punktmasse der immerhin NA Moleküle pro mol zu untersuchen. Die große Zahl erlaubt es uns aber, einen guten Mittelwert zu bilden. Im Klartext heißt das: Für den Zustand eines Idealen Gases ist nur eine statistische Beschreibung über Mittelwertbildungen möglich; diesem Umstand verdankt dieses Themengebiet der Wärmelehre seinen Namen:
Merke: Die kinetische Gastheorie untersucht mit Hilfe der statistischen Mechanik den empirisch gefundenen Zusammenhang von Druck p, Volumen V und Temperatur T. |
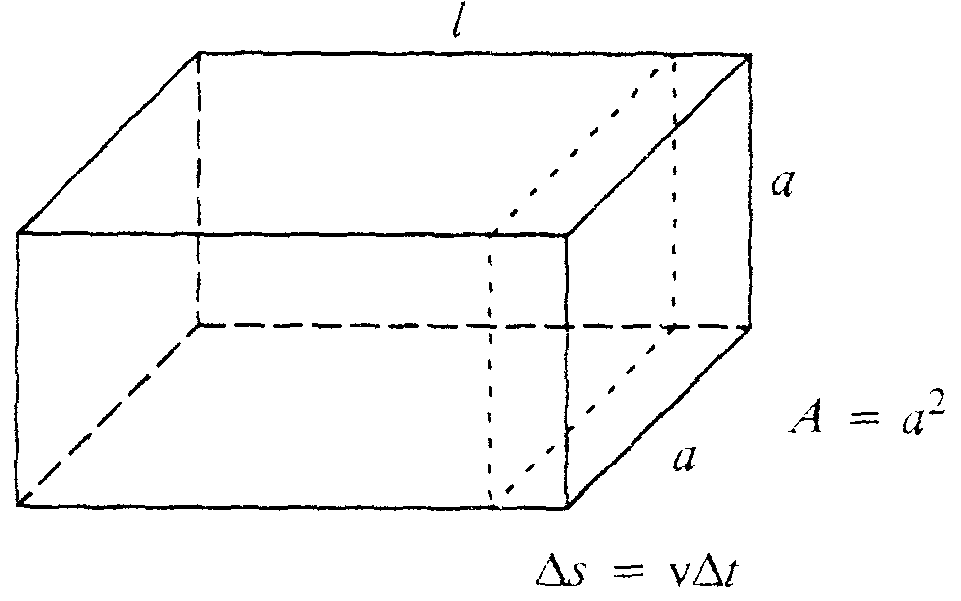
Betrachten wir nun ein Volumen V, in dem sich ein ideales Gas befinde. Der Einfachheit halber wählen wir das Volumen in Form eines Quaders mit quadratischer Stirnfläche a2 und der Länge l . Dann gilt für das Volumen des Quaders
![]()
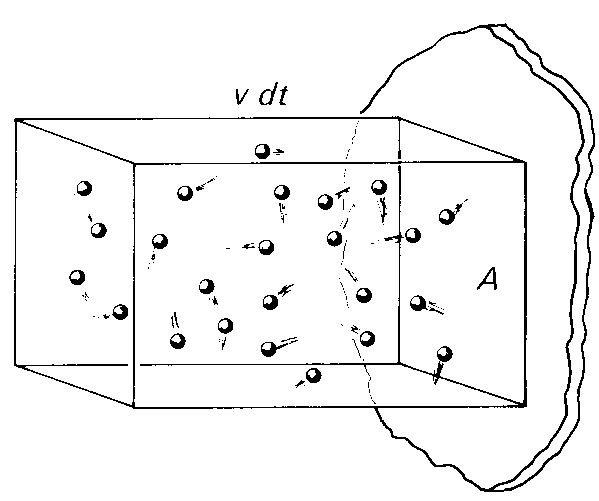
In diesem Volumen bewegen sich N Moleküle der Masse m regellos hin und her.
Wie läßt sich in diesem Modell der Druck auf die Wände des Gefäßes aus der Molekülbewegung herleiten 
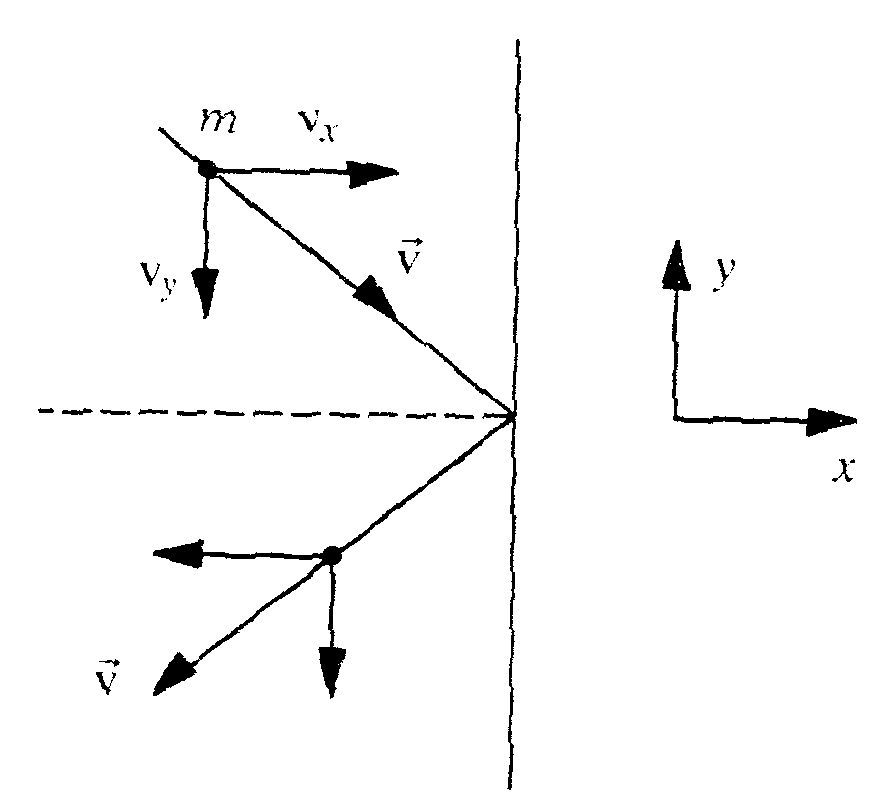
Um diese Frage zu beantworten betrachten wir wie angekündigt zunächst ein Molekül, das auf seinem Flug auf eine Wand trifft. Wir gehen davon aus, daß dieses Molekül nicht senkrecht auf die Wand treffe. Beim Stoß an der Wand wird ein Impuls übertragen, das wissen wir aus der Mechanik. Wir berechnen deshalb den Impuls, weil wir damit über die Beziehung der Kraft als Änderung des Impulses mit der Zeit und schließlich mit der Definition des Druck als Kraft pro Fläche den Druck berechnen wollen.
Die Änderung des Impulses berechnet sich dabei aus
Legen wir nun das Koordinatensystem so, daß die y-Achse längs der angestoßenen Wand verläuft, und die x-Achse senkrecht dazu, so können wir den Geschwindigkeitsvektor geschickt zerlegen: Die y-Komponente der Geschwindigkeitsvektors bleibt beim Stoß erhalten, während die x-Komponente ihr Vorzeichen ändert. Diese Geschwindigkeitsänderung
führt zu einer Impulsänderung
Nun können wir davon ausgehen, daß unser Molekül nicht nur einmal an eine Wand stößt, sondern auf seinem Weg ohne Energieverlust immer wieder Wände treffen wird.
Wie häufig aber trifft unser Molekül auf eine Wand 
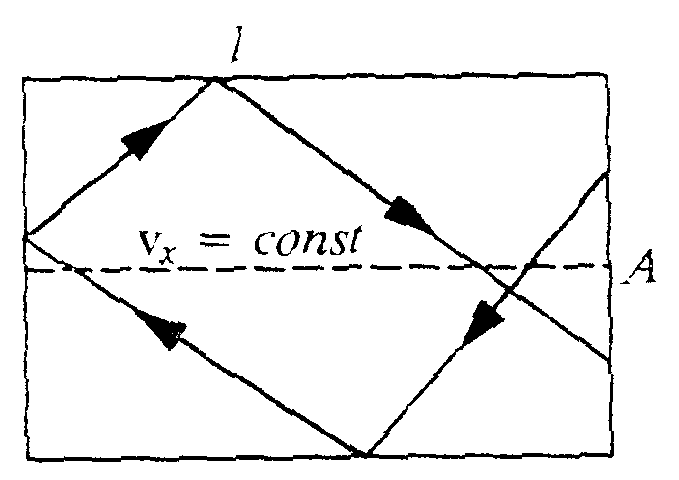
Diese Frage ist einfach zu beantworten: Wir wissen, daß der Betrag der Geschwindigkeit des Moleküls in x-Richtung konstant ist, da die Reflexion immer elastisch erfolgt und die y-Komponente erhalten bleibt. Aus der Mechanik kennen wir das Gesetz für die benötigte Zeit t um eine Strecke x mit konstanter Geschwindigkeit v zurück zulegen.
In unserem Fall muß eine Strecke von der zweifachen Länge l des Quaders zurück gelegt werden, damit das Molekül wieder an dieselbe Wand stößt.
Dann gilt
Die Kraft, die Das Teilchen auf die Fläche A, also eine Wand, ausübt ist dann
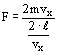
Der Druck auf die Fläche A, der durch unser eines Molekül erzeugt wird ist dann
wegen ![]()
mit V = ![]()
Das kann einfach über Summenbildung berechnet werden:
Nun müssen wir versuchen , diese Summe zu interpretieren. Dazu erweitern wir mit N:
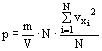
In der Statistik wird die Summe über mehrere Werte geteilt durch die Anzahl der Werte als Mittelwert eingeführt. Damit definieren wir die mittlere Geschwindigkeit als
Definition XI.6: Die mittlere Geschwindigkeit |
Mit dieser Definition folgt
Diese Größe ist eine rein statistische Größe. Wir brauchen jedoch eine meßbare Größe, die uns in Versuchen zugänglich ist.
Mit
gilt auch
Wir nutzen jetzt aus, daß alle drei Raumrichtungen statistisch gleichberechtigt sind, d.h. daß keine Richtung bei der regellosen Bewegung der Moleküle bevorzugt wird.
Dann gilt
Damit folgt aus
direkt
Diese Gleichung wird Grundgleichung der kinetischen Gastheorie genannt.
Grundgleichung der kinetischen Gastheorie: |
Jetzt haben wir den Druck, der auf eine Gefäßwand wirkt, aus der mechanischen Betrachtung der Gasmoleküle erklärt und einen Zusammenhang hergeleitet. Im Anschluß müssen wir uns fragen, wie die Temperatur als Folge der Bewegung der Moleküle aufzufassen ist:
Um diese Frage zu beantworten betrachten wir wieder ein mol eines idealen Gases. Wir haben zwei wichtige Gleichungen kennengelernt:
1. das Idealgasgesetz
2. die Grundgleichung
Diese beiden Gleichungen wollen wir nun vergleichen. Dazu formen wir zunächst das Idealgasgesetz um in die Form
Nun betrachten wir die Grundgleichung der kinetischen Gastheorie für die Stoffmenge 1 mol:
mit N = NA Molekülen in einem mol und dem Volumen Vm, das ein mol einnimmt gilt
Der Vergleich von
¬ und zeigt, daß gilterweitert mit 2
In dieser Gleichung ist der Ausdruck für die mittlere kinetische Energie eines![]() Moleküls enthalten. Mit
Moleküls enthalten. Mit ![]() folgt
folgt
Man faßt nun die beiden Naturkonstanten R und NA zusammen, um die Rechnung mit dieser Gleichung zu vereinfachen
Definition XI.7: Die Boltzmann-Konstante wird definiert als |
Mit dieser Abkürzung folgt
Diese Gleichung gibt den wichtigen Zusammenhang der mittleren kinetischen Energie eines Moleküls mit der Temperatur an. Da dieser Zusammenhang einer der wichtigsten der kinetischen Gastheorie ist, wollen wir ihn näher untersuchen.
Durch diese Beziehungen erhält die absolute Temperatur, die zunächst rein formal zur vereinfachenden Darstellung der Gasgesetze eingeführt wurde, eine anschauliche, physikalische Bedeutung. Offensichtlich wird nicht nur der Druck eines Gases, sondern auch seine Temperatur durch die Bewegungen seiner Teilchen bestimmt.
Dabei kommt es aber nur auf die ungeordnete oder thermische Bewegung der Teilchen an und nicht auf eine allen Molekülen gemeinsame, überlagerte Bewegung. Temperatur und Druck sind statistische Größen, die sich nur auf eine sehr große Anzahl von Teilchen beziehen lassen.
Durch die kinetische Deutung der Temperatur wird jetzt auch die Bezeichnung absoluter Nullpunkt verständlich. Für T = 0 K ist auch ![]() , d.h. die Teilchen sind in Ruhe. Da die kinetische Energie keine negativen Werte annehmen kann, ist dies der kleinste überhaupt möglich Wert.
, d.h. die Teilchen sind in Ruhe. Da die kinetische Energie keine negativen Werte annehmen kann, ist dies der kleinste überhaupt möglich Wert.
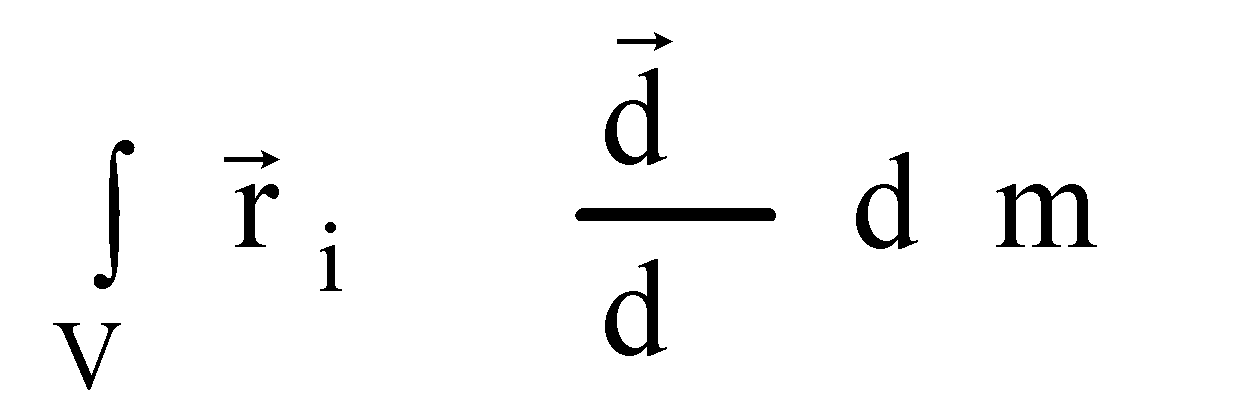
Auf ein einzelnes Teilchen des Gases entfällt der Energieanteil![]() . Da wir festgestellt hatten, daß keine Raumrichtung bevorzugt wird, besitzt jedes Teilchen entsprechend den drei räumlichen Richtungen drei voneinander unabhängige Bewegungsmöglichkeiten. Man sagt kurz: jedes Teilchen besitzt drei Freiheitsgrade der Translation. Besteht das Molekül nicht nur aus einem Atom, so hat es zusätzlich die Bewegungsfreiheit, sich um bestimmte Achsen zu drehen. Ein solches Molekül kann zusätzlich drei Freiheitsgrade der Rotation besitzen, je nachdem, ob die Drehachse raumfest ist (1 Freiheitsgrad) oder ob sie sich in einer Ebene bewegen kann (2 Freiheitsgrade) bzw. ob die Drehachse frei im Raum beweglich ist. Diese Überlegung zu einem späteren Zeitpunkt in der Experimentalphysik vertieft.
. Da wir festgestellt hatten, daß keine Raumrichtung bevorzugt wird, besitzt jedes Teilchen entsprechend den drei räumlichen Richtungen drei voneinander unabhängige Bewegungsmöglichkeiten. Man sagt kurz: jedes Teilchen besitzt drei Freiheitsgrade der Translation. Besteht das Molekül nicht nur aus einem Atom, so hat es zusätzlich die Bewegungsfreiheit, sich um bestimmte Achsen zu drehen. Ein solches Molekül kann zusätzlich drei Freiheitsgrade der Rotation besitzen, je nachdem, ob die Drehachse raumfest ist (1 Freiheitsgrad) oder ob sie sich in einer Ebene bewegen kann (2 Freiheitsgrade) bzw. ob die Drehachse frei im Raum beweglich ist. Diese Überlegung zu einem späteren Zeitpunkt in der Experimentalphysik vertieft.