Merke: Ein Gas des Volumens V0 bei t0 = 0°C erfährt bei konstantem Druck bei Erwärmung um D t = t eine Volumenänderung von |
XI.1 Idealgasgesetze
Versuch IX.1: Nachweis des Boyle-Mariottchen Gesetzes
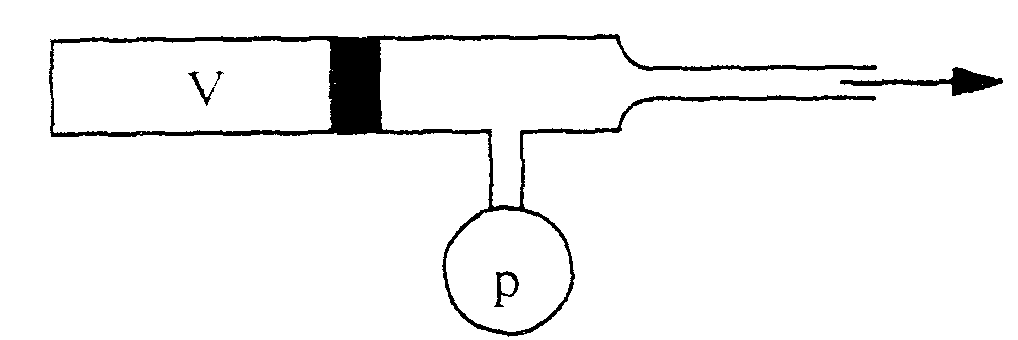 Für diesem Versuchsaufbau benötigen wir einen Zylinder, der mit einem beweglichen Stempel dicht verschlossen ist, und eine Pumpe. In einem Teilraum des Zylinder wird ein ideales Gas eingeschlossen. Die Seite, an der die Pumpe angeschlossen ist, sei mit Luft gefüllt. Jetzt kann mit Hilfe der Pumpe ein Unterdruck im Zylinder erzeugt werden. Auf dem Zylinder sind lineare Markierungen angebracht, so daß das Volumen des eingeschlossenen Gases qualitativ gemessen werden kann. Auch der Druck kann gemessen werden. Nun legt man beliebig eine Anfangsstellung fest. Komprimiert man das Gas, so steigt der Druck an. Umgekehrt hat die Erzeugung von Unterdruck zur Folge, daß das Gasvolumen sich ausdehnt.
Für diesem Versuchsaufbau benötigen wir einen Zylinder, der mit einem beweglichen Stempel dicht verschlossen ist, und eine Pumpe. In einem Teilraum des Zylinder wird ein ideales Gas eingeschlossen. Die Seite, an der die Pumpe angeschlossen ist, sei mit Luft gefüllt. Jetzt kann mit Hilfe der Pumpe ein Unterdruck im Zylinder erzeugt werden. Auf dem Zylinder sind lineare Markierungen angebracht, so daß das Volumen des eingeschlossenen Gases qualitativ gemessen werden kann. Auch der Druck kann gemessen werden. Nun legt man beliebig eine Anfangsstellung fest. Komprimiert man das Gas, so steigt der Druck an. Umgekehrt hat die Erzeugung von Unterdruck zur Folge, daß das Gasvolumen sich ausdehnt.
Empirisch findet man bei diesem Versuch für ideale Gase, daß bei konstanter Temperatur der doppelte Druck aufgewendet werden muß, um das Volumen zu halbieren. Dies gilt natürlich nur, wenn die Menge des Gases konstant gehaltenen wird.
Bis auf Meßungenauigkeiten bei hohen Drucken, wird das Gesetz bestätigt. Die Ungenauigkeiten liegen darin begründet, daß kein ideales Gas verwendet wurde.
Diese Gesetzmäßigkeit hatten wir schon als Gesetz von Boyle-Mariotte oder auch nur Boylesches Gesetz kennengelernt.
Merke: Bei gleicher Menge eines Gases und konstanter Temperatur ist das Produkt aus Volumen und Druck konstant: p × V = const
Boyle-Mariotte |
2.Gesetz für ideale Gase:
In Kapitel X hatten wir für den Zusammenhang zwischen Temperatur und Volumen eines idealen Gases das Gesetz von Gay-Lussac formuliert:
Merke: Ein Gas des Volumens V0 bei t0 = 0°C erfährt bei konstantem Druck bei Erwärmung um D t = t eine Volumenänderung von |
Mit der absoluten Temperatur
folgt aus dem Gesetz
mit T0 = 0°C = 273,15 K
Diese Formel gilt für beliebige Temperaturen T und die dazu gehörigen Volumina V. Bei festem Druck p sind V0 und T0 Konstante. Damit folgt
Dieses Gesetz wird manchmal 1. Gesetz von Gay-Lussac genannt. Es ist nur eine äquivalente Formulierung des bereits bekannten Gesetzes von Gay-Lussac.
Merke: Das 1.Gesetz von Gay-Lussac besagt, daß für ideale Gase bei konstantem Druck |
Der Vergleich der beiden Gesetze zeigt dann eine weiterführende Gesetzmäßigkeit:
Aus
und
folgt
Dieses Gesetz gilt für die feste Menge eines idealen Gases.
Um die folgenden Rechnungen zu vereinfachen, muß eine neue Größe eingeführt werden. Das Modell des idealen Gases läßt bereits vermuten, daß diese Konstanten aus den Gesetzen für ideale Gase von der Anzahl der Moleküle in einem Gasvolumen abhängen. Deshalb definiert man eine Hilfsgröße, die ein Maß dafür ist, wieviele Moleküle in einem Gasvolumen sind. Diese Größe heißt mol und wird aus meßtechnischen Gründen definiert als
Definition XI.1: Ein mol ist die Stoffmenge eines Gases, die ebenso viele Moleküle enthält wie zwölf Gramm C12, nämlich NA. |
In 12 g C12 sind 6,022 1023 Moleküle. Damit entspricht ein mol des Stoffes C12 genau einer Menge von 12 g. Diese Anzahl, die aus meßtechnischen gründen über C12 definiert wurde wird Avogadrosche Zahl genannt.
Definition XI.2: Die Avogadrosche Zahl ist die Anzahl der Moleküle in einem mol. |
Definition XI.3: Die relative Molekülmasse Mr eines Stoffs entspricht einem Zwölftel der Masse von C12 mal der Molekülmasse. 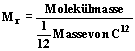 |
Damit entspricht die relative Molekülmasse ungefähr der Summe der Atomgewichte, als z.B. bei H2O ist Mr = 80. Diese Näherung kann gut für Überschläge der Größenordnungen genutzt werden.
Abschließend definiert man die Molmasse M, d.h. die Masse, die ein mol eines Stoffes einnimmt.
Definition XI.4: Die Molmasse M ist das Produkt aus der Masse eines Moleküls und der Anzahl der Moleküle in einem mol. |
Die Einheit der Molmasse ist gebunden an die Dimension.
Abschließend definieren wir noch die Molwärme:
Definition XI.5: Die Molwärme ist das Produkt aus der spezifischen Wärme eines Stoffs und seiner Molmasse: Molwärme = Mc. |
Mit Hilfe dieser Größen wollen wir nun die Proportionalitätskonstante aus dem Gesetz
bestimmen. Dabei bezeichnen wir die Größen, die sich auf die Stoffmenge von einem mol beziehen nun mit dem Index m .
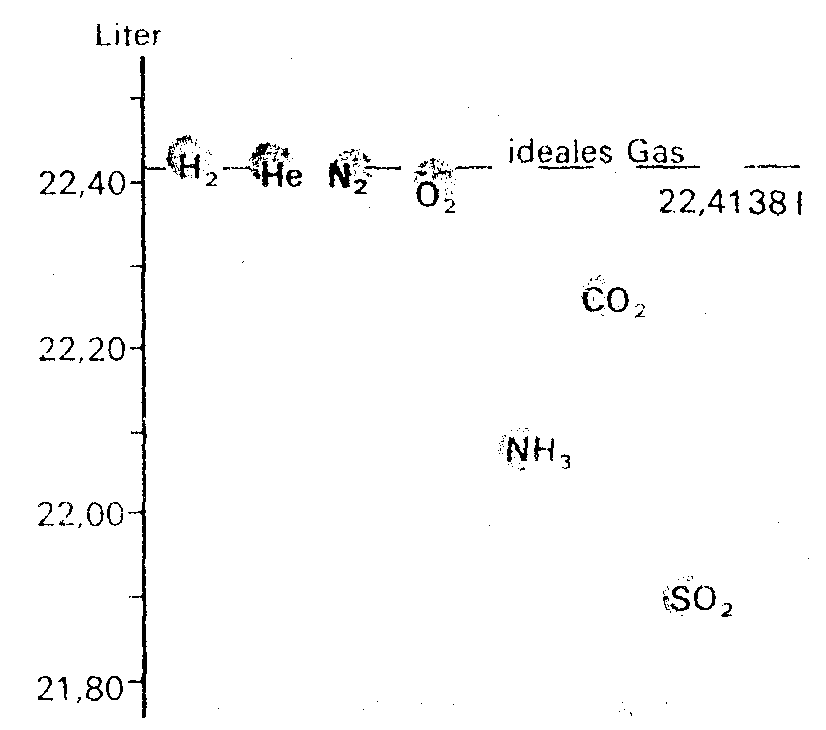
Eine Konsequenz des Gesetzes ist, daß ein mol eines idealen Gases unter gleichen Bedingungen immer das gleiche Volumen Vm annimmt. Unter Normalbedingungen, d.h.
beträgt dieses Volumen
Dieses Volumen nennt man molares Normvolumen.
Merke: Ein mol eines idealen Gases nimmt bei T0= 273,15 K und p0 = 101,325 kPa das molare Normvolumen |
Das Volumen für n mol berechnet sich dann als
damit ergibt sich aus
mit V0 = ![]() n
n
Der Vergleich mit der ursprünglichen Gleichung zeigt, daß ![]() unsere gesuchte Konstante ist. Damit läßt sich diese Naturkonstante berechnen. Sie wird universelle Gaskonstante genannt und mit R bezeichnet.
unsere gesuchte Konstante ist. Damit läßt sich diese Naturkonstante berechnen. Sie wird universelle Gaskonstante genannt und mit R bezeichnet.
Merke: Die universelle Gaskonstante R = |
bzw. in nicht SI-Einheiten R = ![]() .
.
Damit können wir das Gesetz jetzt formulieren:
<
oder mit V = Vm n
Dieses Gesetz hatten wir Idealgasgesetz genannt
Idealgasgesetz:
|
Dieses Gesetz enthält bereits alles, was wir für die Zustandsberechnung idealer Gase wissen muß. Es sei noch einmal erwähnt, daß diese Gesetzmäßigkeiten streng genommen nur für ideale Gase gelten, aber auch eine gute Näherung für reale Gase sind, solange diese ausreichend verdünnt sind. Dann ist das Volumen von einem mol groß und folglich die Temperatur hoch und der Druck klein.
Umgekehrt kann man nun aus dem Idealgasgesetz die beiden anfangs zugrunde gelegten Gesetze für ideale Gase und noch ein weiteres Gesetz ableiten.
Betrachten wir zunächst das Boyle-Mariott'sche Gesetz:
Gegeben sei
Dann folgt aus
mit R, n und T = const
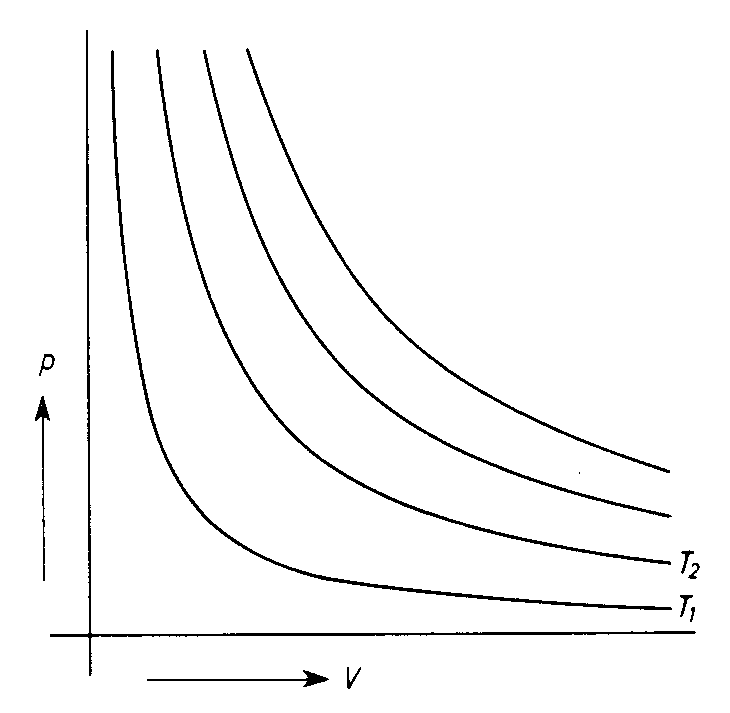
Im p/V-Diagramm führt die Gleichung ![]() zu Hyperbeln, die je nach Temperatur T steiler oder flacher verlaufen. Je größer T ist, desto größer ist auch
zu Hyperbeln, die je nach Temperatur T steiler oder flacher verlaufen. Je größer T ist, desto größer ist auch ![]() ; die Hyperbeln sind steiler. Diese Graphen der Gleichung des Boyle-Mariott'schen Gesetzes werden Isotherme genannt.
; die Hyperbeln sind steiler. Diese Graphen der Gleichung des Boyle-Mariott'schen Gesetzes werden Isotherme genannt.
Merke: Der 1.Spezialfall des Idealgasgesetzes ist das Boyle-Mariott'sche Gesetz mit T = const. Der hyperbelförmige Graph im p/V-Diagramm wird Isotherme genannt.. |
Betrachten wir nun das 1. Gesetz von Gay-Lussac:
Gegeben sei
Dann folgt aus
mit R, n und p = const
Mit der obigen Rechnung folgt daraus auch die Gleichung
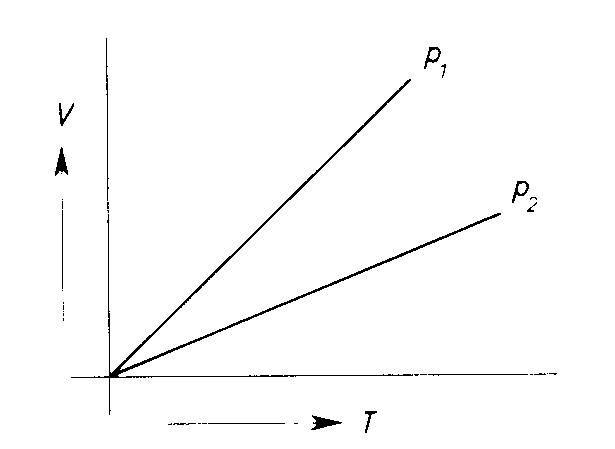
Im V/T-Diagramm führt die Gleichung ![]() zu Graden, die je nach Druck p steiler oder flacher verlaufen. Je kleiner p ist, desto größer ist V(T); die Graden sind steiler. Diese Graphen der Gleichung des 1. Gesetzes von Gay-Lussac werden Isobare genannt.
zu Graden, die je nach Druck p steiler oder flacher verlaufen. Je kleiner p ist, desto größer ist V(T); die Graden sind steiler. Diese Graphen der Gleichung des 1. Gesetzes von Gay-Lussac werden Isobare genannt.
Merke: Der 2.Spezialfall des Idealgasgesetzes ist das 1. Gesetz von Gay-Lussac mit p = const.
Der lineare Graph im V/T-Diagramm wird Isobare genannt. |
Abschließend berechnen wir, was bei konstantem Volumen aus der Idealgasgleichung folgt:
Gegeben sei
mit R, n und V = const
Û ![]()
Eine analoge Rechnung zu oben liefert daraus die Gleichung
Dieses Gesetz wird 2.Gesetz von Gay-Lussac genannt.
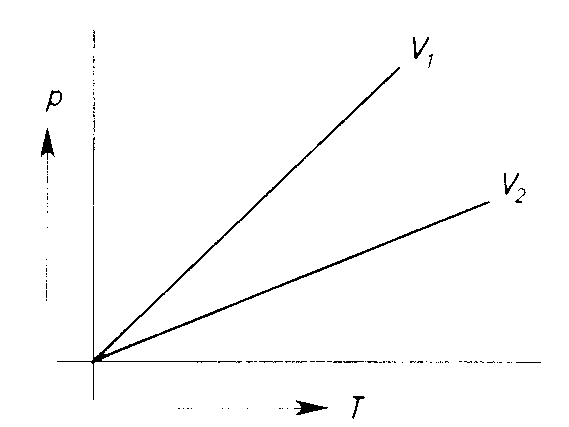
Im p/T-Diagramm führt die Gleichung ![]() zu Graden, die je nach Volumen V steiler oder flacher verlaufen. Je kleiner V ist, desto größer ist V(T); die Graden sind steiler. Diese Graphen der Gleichung des 2. Gesetzes von Gay-Lussac werden Isochore genannt.
zu Graden, die je nach Volumen V steiler oder flacher verlaufen. Je kleiner V ist, desto größer ist V(T); die Graden sind steiler. Diese Graphen der Gleichung des 2. Gesetzes von Gay-Lussac werden Isochore genannt.
Merke: Der 3.Spezialfall des Idealgasgesetzes ist das 2. Gesetz von Gay-Lussac mit p = const.
|