XI.3 Geschwindigkeitsverteilung
Die Gleichung besagt
Û ![]()
mit k = ![]()
mit der Molmasse M = mNA
Bei einer Temperatur von T = 293 K, also t = 20░C, und einer Molmasse M = 32 ![]() entspricht das einer Geschwindigkeit
entspricht das einer Geschwindigkeit ![]() für O2
für O2
bzw.
Die Geschwindigkeitsverteilung wurde erstmals 1920 von dem deutschen Physiker Otto Stern ausgeführt.
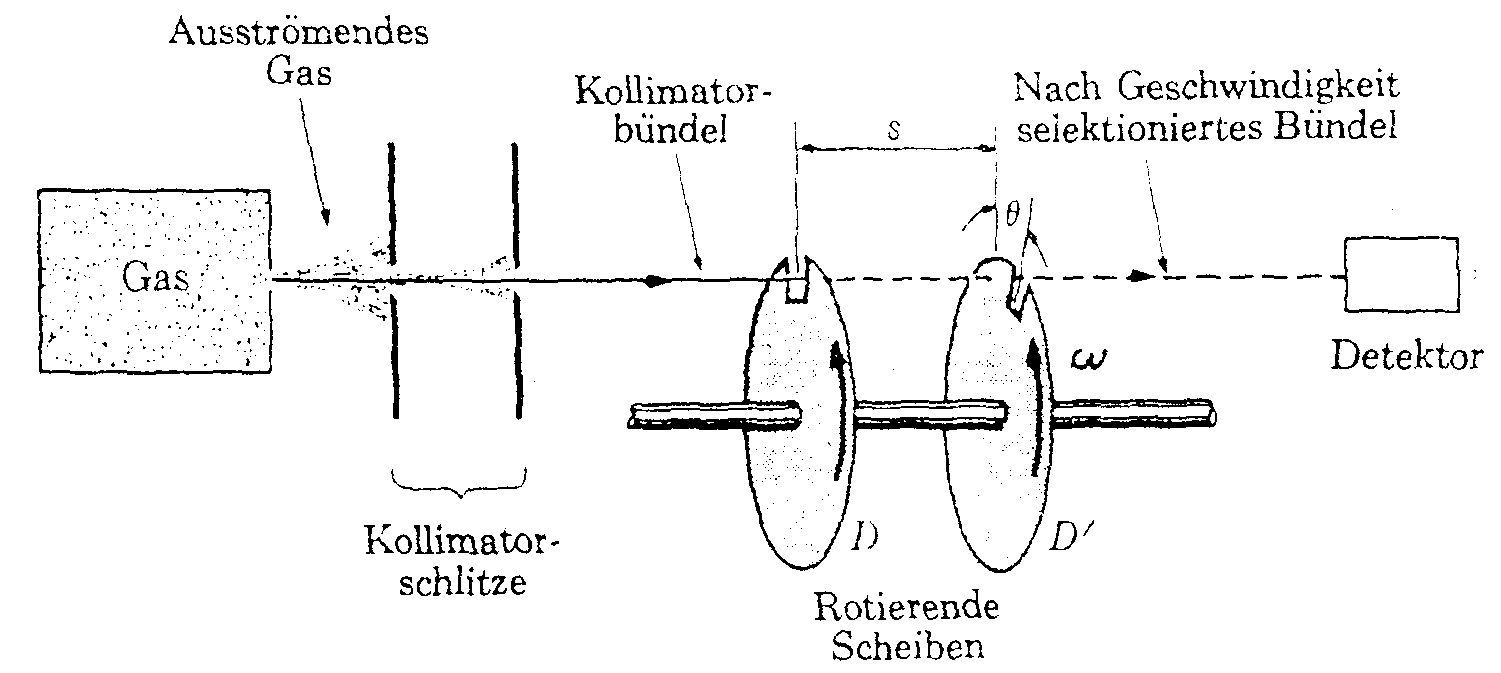
Prinzip dieses Versuchs ist es, die Geschwindigkeit eines scharf begrenzten Molekular- oder Atomstrahls zu messen. Zu diesem Zweck läßt man Gas aus einem Behälter strömen. Dieses strömende Gas wird durch zwei Kollimatorschlitze gebündelt. Die Geschwindigkeit dieser Atome kann man sehr einfach mit zwei Zahnrädern, die im Abstand s auf einer gemeinsamen Achse so montiert sind, daß ein Teilchen die ruhenden Scheiben durch die Löcher passieren kann, messen. Passiert ein Teilchen die erste Scheibe, so legt es danach einen Weg s zurück bis zur zweiten Scheibe. Diese befindet sich aber nicht in Ruhe sondern rotiert mit der Winkelgeschwindigkeit w .Das zweite Loch ist also gegenüber dem ersten Loch um den Winkel Q verschoben. Für die zur Drehung benötigte Zeit gilt dann t = Q w . In dieser Zeit hat das Teilchen die Strecke s zurückgelegt mit der konstanten Geschwindigkeit v, also gilt t = ![]() . Ein Vergleich dieser beiden Beziehungen zeigt, daß die Geschwindigkeit v des Moleküls oder Atoms zu berechnen ist aus
. Ein Vergleich dieser beiden Beziehungen zeigt, daß die Geschwindigkeit v des Moleküls oder Atoms zu berechnen ist aus ![]() . Variiert man nun die Winkelgeschwindigkeit, so kann man mit einem Detektor messen, mit welcher Geschwindigkeit v wieviele Teilchen fliegen.
. Variiert man nun die Winkelgeschwindigkeit, so kann man mit einem Detektor messen, mit welcher Geschwindigkeit v wieviele Teilchen fliegen.
Dieser Versuch ist leider sehr empfindlich und in der Vorlesung nicht nachzumachen. Deshalb betrachten wir einen Versuch mit unserem 'Gasmodell'. Dabei können wir die Geschwindigkeitsverteilung betrachten und zudem nachweisen, daß unser Modell auch in diesem Aspekt die Wirklichkeit ganz gut beschreibt.
Versuch XI.1: Geschwindigkeitsverteilung
Bei unserem Versuch wird ein Glaszylinder mit leichten Kugeln gefüllt und auf eine Rüttelplatte gestellt. Ein frei beweglicher Stempel drückt im Ruhezustand auf die Kugeln. In dieser Stellung kann man ablesen, welches Volumen die nicht-bewegten 'Gasmoleküle' einnehmen.
Im ersten Versuchsteil betrachten wir den Stempel, während wir die Rüttelplatte starten und damit die Gasmoleküle in Bewegung versetzen. Wir beobachten, daß der Stempel steigt. Offensichtlich erzeugt unser 'Gas' einen Druck auf das Gefäß.
Im zweiten Teil öffnen wir ein kleines Loch an einer Seite des Zylinders. Durch dieses Loch verlassen nun gelegentlich Kugeln das Gefäß. Ein Sortiergerät neben dem Gefäß fängt die Kugel auf und zeigt damit die Häufigkeit der Flugweite, sprich der Geschwindigkeit.
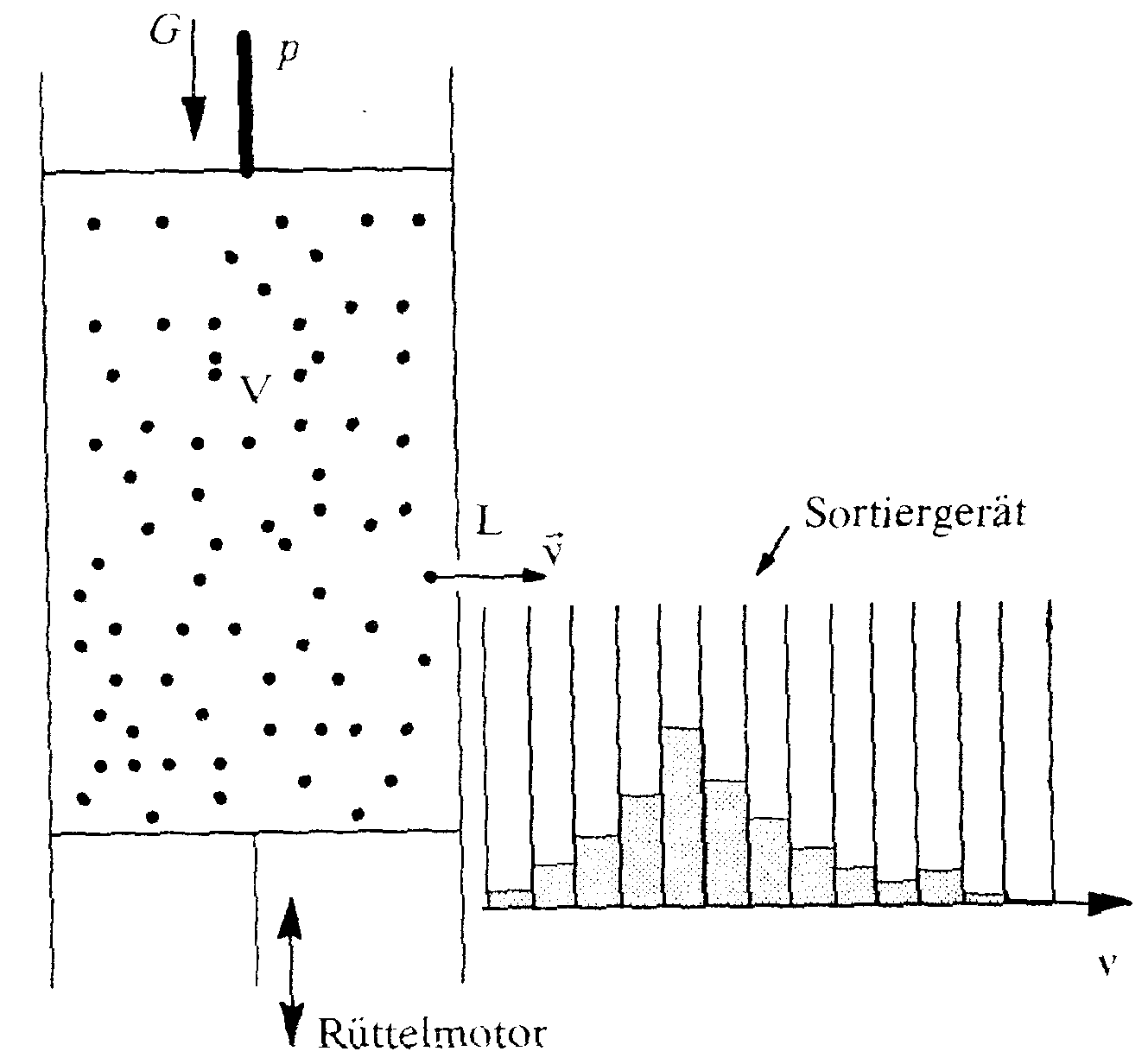
Läuft der Versuch eine längere Zeit, so beobachtet man die in der Abbildung gezeigte Verteilung.
Im letzten Versuchsteil wollen wir das Boyle-Mariott'sche Gesetz bewahrheiten. Hierzu legen wir verschiedene Massen auf den Stempel und messen bei gleicher Rüttelbewegung das Volumen des Gases mittels einer auf den Zylinder gezeichneten Skala. Da der Druck des Gases durch die Rüttelplatte gleich bleibt, der Druck durch die Gewichte jedoch vergrößert wird, muß das Volumen sich verringern. Berücksichtigt man bei der Berechnung des Produktes von Volumen und Gesamtdruck das anfänglich gemessene Eigenvolumen des Gases, so kann man mit diesem Aufbau das Boyle-Mariott'sche Gesetz auf 10% genau bestätigt finden.
Die Geschwindigkeitsverteilung für ideale Gase haben alle ein charakteristische Form. Die Geschwindigkeitsverteilung ist von der Temperatur abhängig: Je größer die Temperatur und damit die kinetische Energie der Moleküle ist, desto weiter fliegen sie. Bevor wir die Geschwindigkeitsverteilung jedoch genau herleiten und interpretieren, betrachten wir zuvor qualitativ die Geschwindigkeitsverteilung n(v) zweier idealer Gase:
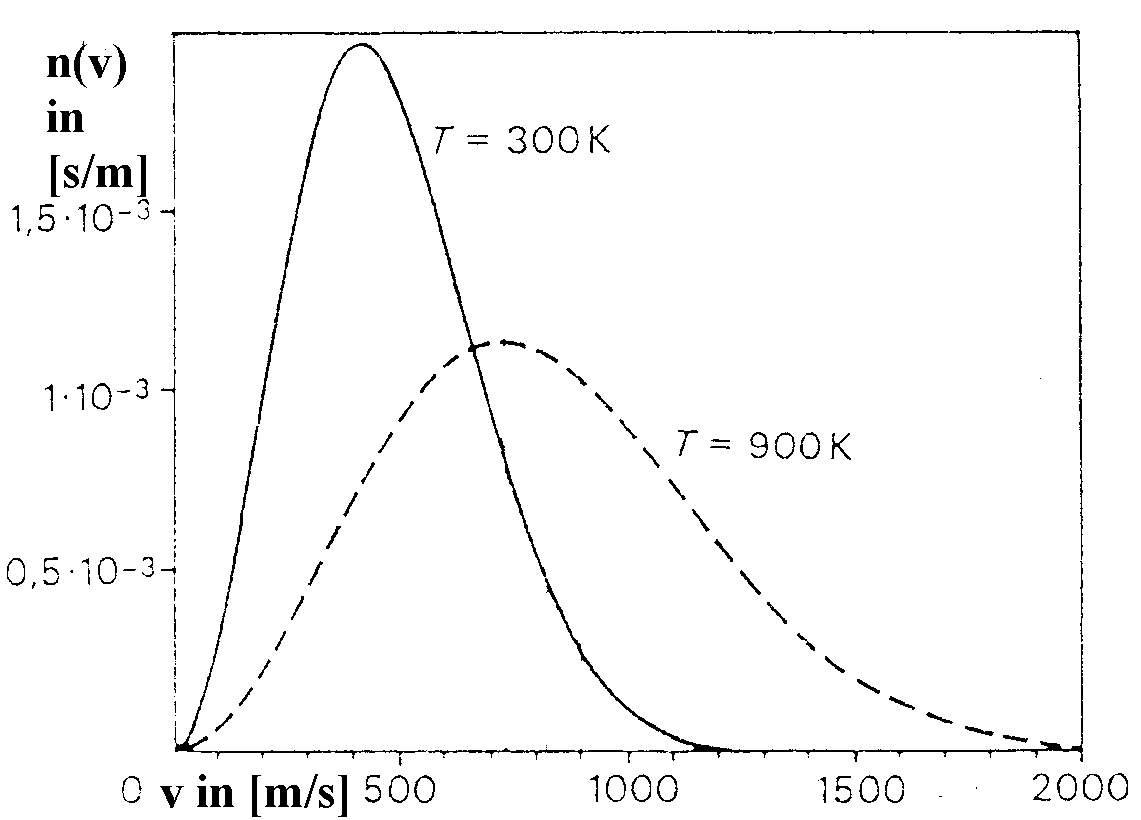
Geschwindigkeitsverteilung n(v) von Stickstoff-Molekülen
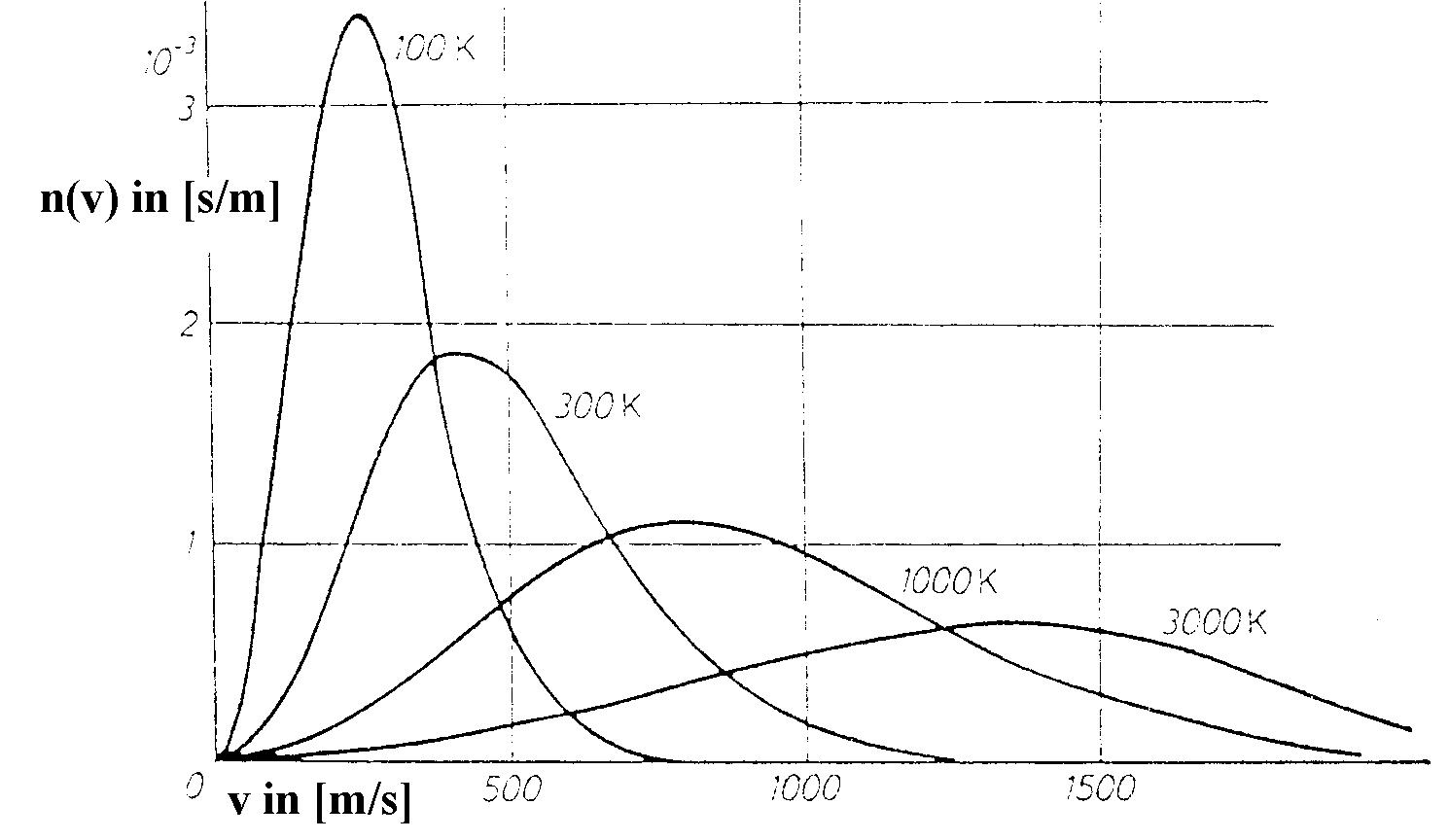
Geschwindigkeitsverteilung n(v) von Luft-Molekülen
Unabhängig von der Verschiebung durch die Temperatur kann man den beiden Diagrammen eine charakteristische Form der Graphen entnehmen. Unterhalb der häufigsten Geschwindigkeit, d.h. im ansteigenden Teil des Graphen verläuft dieser parabolisch. Hier scheint n(v) ~ v2 zu sein. Im fallenden Teil des Graphen sieht man einen exponentiellen Verlauf, also n(v) ~ e-.