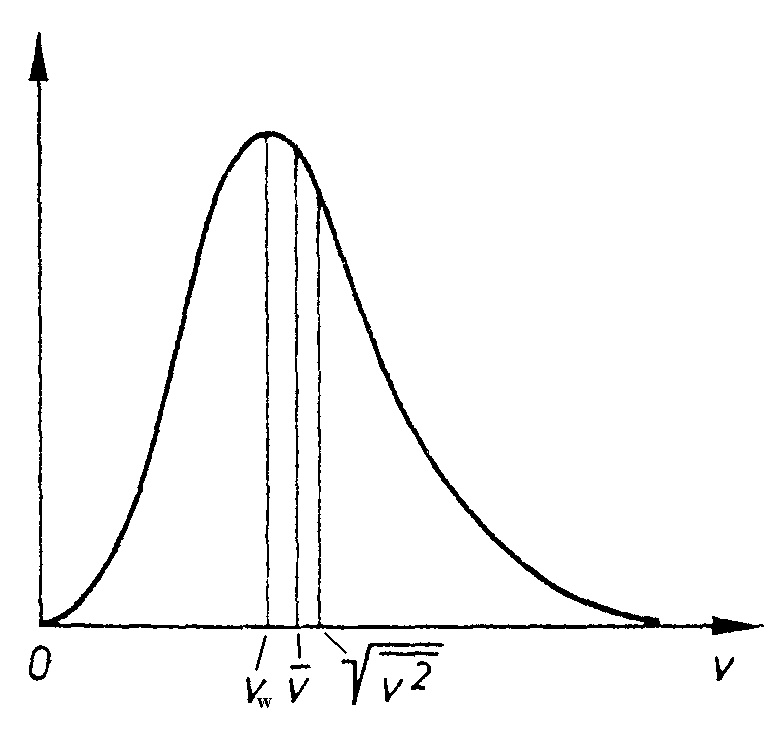
XI.4 Theoretische Berechnung von n(v)
Mithilfe der Idealgasgesetze können wir den Exponenten umformen, wobei wir zunächst annehmen, es handele sich um ein mol Gas. Dann folgt mit dem Volumen eines mol Vm ,der Masse M eines mol des Gases und der Masse m eines Moleküls
mit ![]()
mit ![]()
mit dem Idealgasgesetz für ein mol
![]()
![]()
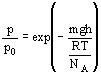
mit ![]()
Der Ausdruck mgh gibt die potentielle Energie WP eines Moleküls im Schwerefeld wieder.
Mit ![]()
Nun schreiben wir noch den Druck p um, indem wir die Teilchenzahldichte betrachten. Dabei definieren wir die Teilchenzahldichte n in Analogie zur Massendichte als Quotient aus den in einem Volumen V enthaltenen Teilchen N und dem Volumen.
Definition XI.8: Die Teilchenzahldichte n ist der Quotient aus den in einem Volumen V enthaltenen Teilchen N und dem Volumen: |
Bei konstanter Temperatur ist die Teilchenzahldichte n proportional zum Druck, da ![]() ~ N ist bei konstantem T. Betrachten man ferner die Masse M als konstant, so folgt
~ N ist bei konstantem T. Betrachten man ferner die Masse M als konstant, so folgt
Diese Gleichung ist die Boltzmann-Verteilung.
Merke: Das Verhältnis der Teilchenzahldichte von der potentielle Energie der Moleküle eines idealen Gases wird gegeben durch die Boltzmann-Verteilung |
Anders ausgedrückt gibt diese Gleichung wieder, wie die Teilchenzahldichten n und n0 sich verhalten, wenn sie an diesen Orten die potentielle Energie W und W0 haben. Potentielle Energie kann dabei Schwereenergie, aber auch z.B. elektrische Energie sein. Deshalb formuliert man für allgemeine Energiezustände Wi eine Aussage über die Wahrscheinlichkeit, mit der Gasmoleküle eines Systems diese Energie besitzen:
Merke: Wenn die Moleküle eines Systems bei der Temperatur T verschiedene Energien Wi einnehmen können, dann geschieht das mit der Wahrscheinlichkeit pi :
|
Dabei ist gi das statistische Gewicht des Zustandes i. Verschiedene Zustände haben verschiedene statistische Gewichte, wenn ihre Wahrscheinlichkeit schon abgesehen von allen energetischen Betrachtungen verschieden sind. Diese Gleichung wird zentrales Theorem der statistischen Mechanik genannt:
Zentrales Theorem der statistischen Mechanik:
|
Mit dieser Gleichung läßt sich die Geschwindigkeitsverteilung von Gasmolekülen berechnen:
Für die Moleküle der Masse m eines Gases kann man die kinetische Energie angeben mit
Nach Boltzmann nehmen diese Moleküle diese Energie mit einer Wahrscheinlichkeit ein von
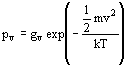 .
.Der Index v bezeichnet hier die Abhängigkeit der Energiezustände von der Geschwindigkeit v. Das statistische Gewicht gv ist in diesem Fall die Zahl der mögliches Zustände mit einer Geschwindigkeit zwischen v und v + dv. Bei diesem Ansatz wurde bedacht, daß eine exakte Geschwindigkeit v nicht zu bestimmen ist, sondern immer mit eine Ungenauigkeit dv behaftet ist. Betrachtet man nun den Geschwindigkeitsraum, d.h. den Raum, der durch die Geschwindigkeitskomponenten vx , vy und vz aufgespannt wird, so beschreiben die Vektoren ![]() und
und ![]() zwei konzentrische Kugelschalen. Das kann man sich mit einer Skizze veranschaulichen: Nur die Länge der Vektoren
zwei konzentrische Kugelschalen. Das kann man sich mit einer Skizze veranschaulichen: Nur die Länge der Vektoren ![]() und
und ![]() sind bekannt. Die Zahl der möglichen Zustände mit einer Geschwindigkeit zwischen v und v + dv entspricht also der Anzahl der Punkte zwischen diesen Kugelschalen, also dem eingeschlossenen Volumen.
sind bekannt. Die Zahl der möglichen Zustände mit einer Geschwindigkeit zwischen v und v + dv entspricht also der Anzahl der Punkte zwischen diesen Kugelschalen, also dem eingeschlossenen Volumen.
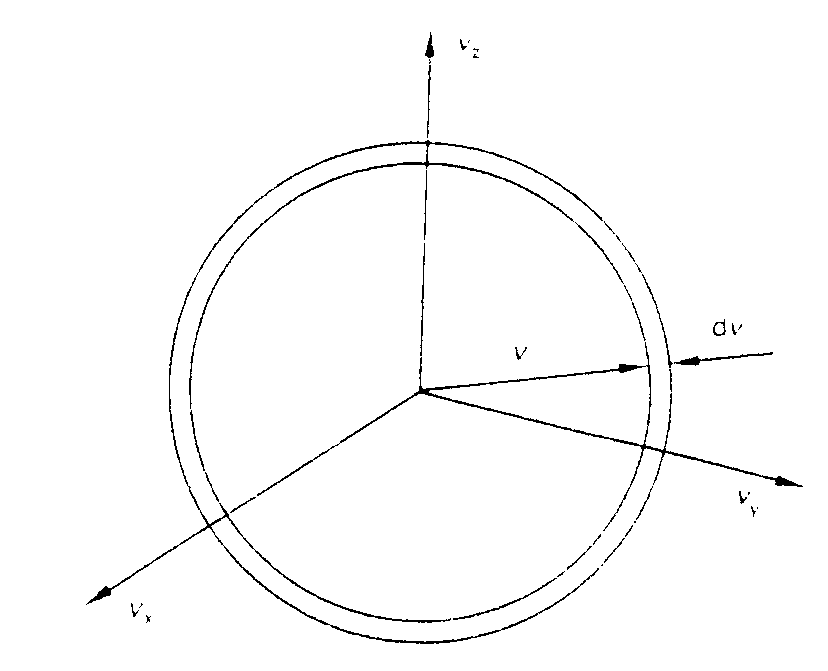
Also gilt mit
Für uns ist jedoch nicht die Wahrscheinlichkeit interessant sondern die wirkliche Verteilung, deshalb betrachten wir N(v), wobei N(v) ~ pv ist.
mit ![]() folgt
folgt
mit der Proportionalitätskonstanten C.
Die Gesamtzahl der Teilchen muß erhalten bleiben, also muß gelten:
also folgt
Die Lösung des Integrals über Substitution ergibt die
Maxwellsche Geschwindigkeitsverteilung:
|
Die exakte Rechnung kann im Anhang nachgelesen werden.
Wichtig an dieser Stelle ist es vor allem, den quadratischen Term und den exponentiellen Term zu erkennen. Diese beiden Faktoren hatten wir aus dem Diagramm bereits abgelesen. Ferner ist wichtig zu wissen, daß der Boltzmannfaktor in dieser Gleichung steht und wie die Gleichung entsteht.
Diese Bewegung ist unter einem Mikroskop deutlich zu beobachten. Auf diese Weise stieß der Botaniker Brown, der zunächst aufgrund der regellosen, zuckenden Bewegungen die Schwebeteilchen in Pflanzenzellen für Lebewesen hielt, 1827 auf einen direkten Beweis der kinetischen Gastheorie.
Wir wollen die Brownsche Molekularbewegung anhand unseres Gasmodells und anschließend in einem Film betrachten:
Versuch XI.2: Brownsche Molekularbewegung
Für diese Demonstration geben wir zu den kleinen 'Gasmolekülen' noch größere Schwebeteilchen, in unserem Fall größere Styroporkugeln in den Zylinder. Versetzt man die Moleküle jetzt mit Hilfe der Rüttelplatte in Bewegung, so kann man beobachten, daß die kleinen Kugeln bald zu schnell werden, um sie mit bloßem Auge aufzulösen. Die größeren Kugeln hingegen fliegen so langsam, daß man ihre Bahn mühelos verfolgen kann.Eine Filmaufnahme zeigt die Bewegung von Fetttropfen einer Milchemulsion unter dem Mikroskop und die Molekularbewegung von Bakterien.
Bisher haben wir einen Mittelwert der Geschwindigkeit definiert und diesen stets als den Mittelwert bezeichnet. Tatsächlich unterscheidet man in den Naturwissenschaften zwischen verschiedenen Mittelwerten. Deshalb muß man genau unterscheiden, um welchen Mittelwert es sich bei einer Rechnung handelt.
Der am häufigsten genutzte Mittelwert, der zudem meist gemeint ist, wenn der Begriff nicht weiter spezifiziert wird, ist der
Diesen hatten wir definiert als
Die Bedingung
liefert
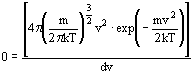
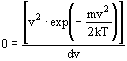
mit ![]()
mit ![]()
Damit schreibt man die
als
Ein Vergleich der beiden mittleren Geschwindigkeiten zeigt:
mit ![]() in der Gleichung
in der Gleichung
und der Gleichung
folgt
und
Damit gilt
Mit dieser Beziehung kann man die Maxwellsche Geschwindigkeitsverteilung besser schreiben als
Als dritte Möglichkeit der Mittelwertbildung definiert man die mittlere Geschwindigkeit als Mittelwert der Verteilung n(v). Damit ist die
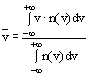 .
.Mit der bereits eingeführten Normierung ![]()
folgt
Eine analoge Rechnung zur Berechnung der Geschwindigkeitsverteilung und der Vergleich mit der wahrscheinlichsten Geschwindigkeit vw führt zu dem Ergebnis
Die Lage der verschieden definierten mittleren Geschwindigkeiten sind in diesem Diagramm aufgetragen: