



Definition IIX.1: Ein Ideales Gas ist ein Gas, in dem die zwischenmolekularen Kräften null sind. |
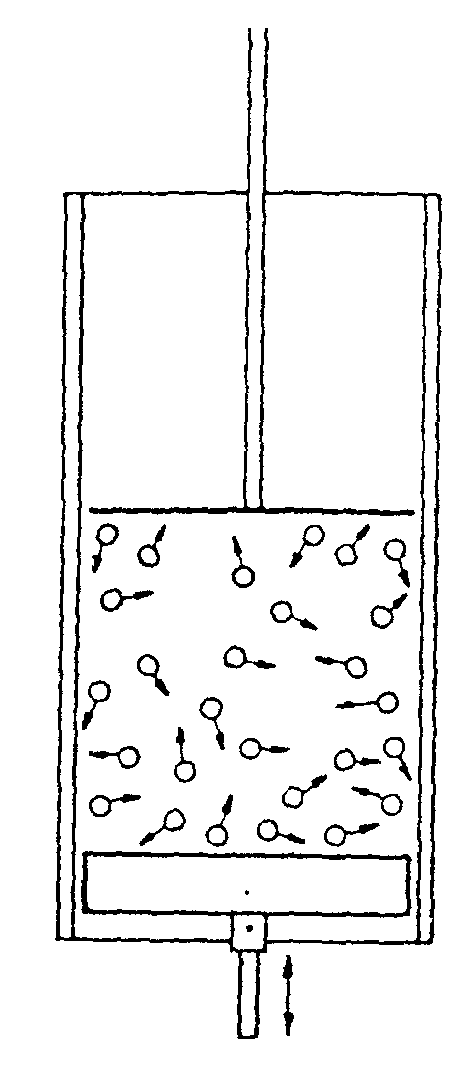 Als Modell eines idealen Gases kann man sich ein geschlossenes Volumen vorstellen, in dem elastische Kugeln ohne sich zu berühren regellose Bewegungen ausführen.
Als Modell eines idealen Gases kann man sich ein geschlossenes Volumen vorstellen, in dem elastische Kugeln ohne sich zu berühren regellose Bewegungen ausführen.
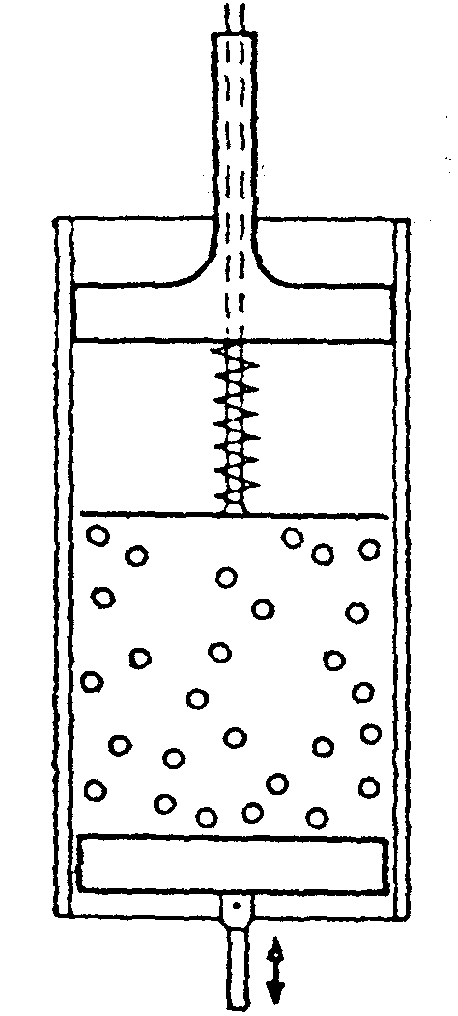 Selbstverständlich sind die Kugeln nicht immer gleichmäßig über den Raum verteilt. Stellt man sich dem Druck nun so vor, daß die Kugeln an die Gefäßwand treffen, so folgt aus dieser ungleichen Verteilung eine statistische Schwankungen der Kraft, die ein eingesperrtes Gas auf einen Kolben ausübt.
Die Druckausbreitung in Gasen erfolgt, genauso wie die Druckausbreitung in Flüssigkeiten, in alle Richtungen gleich.
Da zwischen den Molekülen eines Gases im idealen Fall keine Abstoßungskräfte mehr wirken, lassen sich Gase im Vergleich zu Flüssigkeiten sehr stark zusammendrücken. Die Kompressibilität ist sehr groß, sie haben jedoch keine Volumenelastizität mehr. Die Erfahrung zeigt, daß man trotzdem einen nicht unerheblichen Druck aufwenden muß, um das Volumen eines Gases zu ändern.
Empirisch findet man für ideale Gase, daß bei konstanter Temperatur der doppelte Druck aufgewendet werden muß, um das Volumen zu halbieren. Dies gilt natürlich nur, wenn die Menge des Gases konstant gehaltenen wird.
Diese Gesetzmäßigkeit wird Gesetz von Boyle-Mariotte oder auch nur Boylesches Gesetz genannt.
Selbstverständlich sind die Kugeln nicht immer gleichmäßig über den Raum verteilt. Stellt man sich dem Druck nun so vor, daß die Kugeln an die Gefäßwand treffen, so folgt aus dieser ungleichen Verteilung eine statistische Schwankungen der Kraft, die ein eingesperrtes Gas auf einen Kolben ausübt.
Die Druckausbreitung in Gasen erfolgt, genauso wie die Druckausbreitung in Flüssigkeiten, in alle Richtungen gleich.
Da zwischen den Molekülen eines Gases im idealen Fall keine Abstoßungskräfte mehr wirken, lassen sich Gase im Vergleich zu Flüssigkeiten sehr stark zusammendrücken. Die Kompressibilität ist sehr groß, sie haben jedoch keine Volumenelastizität mehr. Die Erfahrung zeigt, daß man trotzdem einen nicht unerheblichen Druck aufwenden muß, um das Volumen eines Gases zu ändern.
Empirisch findet man für ideale Gase, daß bei konstanter Temperatur der doppelte Druck aufgewendet werden muß, um das Volumen zu halbieren. Dies gilt natürlich nur, wenn die Menge des Gases konstant gehaltenen wird.
Diese Gesetzmäßigkeit wird Gesetz von Boyle-Mariotte oder auch nur Boylesches Gesetz genannt.
Gesetz von Boyle-Mariotte: Bei gleicher Menge eines Gases und konstanter Temperatur ist das Produkt aus Volumen und Druck konstant: p × V = const. |
Merke: Die Kompressibilität idealer Gase ist gleich dem Kehrwert des komprimierenden Drucks: k = 1/p |
Versuch IIX.8: Magdeburger Halbkugeln
 Da wir in der Vorlesung keine Pferde zur Verfügung haben, müssen wir den Versuch mit Professoren durchführen. Um die Proportion zu wahren, verwenden wir natürlich kleinere Halbkugeln. Doch auch unseren Professoren gelingt es nicht, die Halbkugeln gegen den Luftdruck auseinander zu ziehen.
Da wir in der Vorlesung keine Pferde zur Verfügung haben, müssen wir den Versuch mit Professoren durchführen. Um die Proportion zu wahren, verwenden wir natürlich kleinere Halbkugeln. Doch auch unseren Professoren gelingt es nicht, die Halbkugeln gegen den Luftdruck auseinander zu ziehen.
Versuch IIX.9: Messung des Drucks