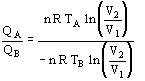XIV.7 Thermodynamische Temperatur
Bei der Herleitung des Wirkungsgrades des Carnot - Prozesses hatten wir festgestellt, daß der Wirkungsgrad nur von der Temperatur der beteiligten Wärmebäder abhängig ist, aber nicht vom Arbeitsmedium:
h Carnot =
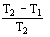
.
Somit ist eine Temperaturdefinition möglich, die unabhängig von speziellen Thermometereigenschaften ist, z.B. Gasthermometer bei tiefen Temperaturen. Betrachten wir hierzu beim Carnot-Prozeß die isothermen Zustandsänderungen
1. isotherme Expansion
Q
A = n R T
A ln
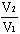
> 0
¬ '
3. isotherme Kompression
Q
B = n R T
B ln
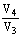
< 0
® ',
Mit der in der Berechnung der Arbeitsbilanz (vgl. Kapitel XIV.1.3) hergeleiteten Beziehung
ergibt sich:
Û 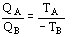
Û T
B =
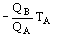
Û 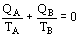
Diese Gleichungen definieren nach William Lord Kelvin die thermodynamische Temperatur.
Die bereits kennengelernte Definition der Temperatur über eine Quecksilbersäule oder ein Gasthermometer hat den Nachteil, daß sie von den Eigenschaften der Thermometersubstanz abhängig sind. Dieser Nachteil kann nun mit Hilfe dieses Ergebnisses aus dem Carnot-Prozess vermieden werden. Aus dem Wirkungsgrad kann man mit dieser Gleichung unmittelbar das Verhältnis der absoluten Temperaturen der beiden Wärmespeicher berechnen. Dann ist die Temperaturskala eindeutig festgelegt, wenn man einen absoluten Fixpunkt definiert. Dazu hat man wie bereits erläutert den Trippelpunkt des Wasser genutzt. Die so festgelegte Temperaturskala nennt man thermodynamisch definierte Temperatur. Sie stimmt praktisch mit der durch ein Gasthermometer festgelegten Temperatur überein.
Desweiteren erlauben diese Beziehungen die Definition einer neuen Zustandsgröße, der Entropie S, die wir im nächsten Kapitel einführen werden.