XIV.5 Zustandsänderung idealer Gase
Allgemein unterscheidet man umkehrbare oder reversible Prozesse und irreversible Prozesse. Irreversibel ist ein Prozess dann, wenn er auf keine Weise vollständig rückgängig gemacht werden kann. Reversibel ist ein Prozeß folglich dann, wenn man ein System dadurch in den Anfangszustand zurückversetzen kann, daß man alle Zustände in umgekehrter Reihenfolge durchläuft.
Reversible Prozesse sind idealisierte Prozesse: es darf weder Reibung existieren, noch darf Wärme an die Umgebung abgegeben werden. Das ist nur möglich, wenn die Zustandsänderung sehr langsam erfolgt.
Merke: Reversibel oder umkehrbare Prozesse sind Prozesse, bei denen die vorgenommene Zustandsänderung zurückgenommen werden kann, ohne daß eine Veränderung bleibt. Reversible Prozesse sind idealisiert. |
Merke: Irreversibele Prozesse sind alle realen Prozesse. Die Umwandlung erfolgt nicht umkehrbar, z.B. die Expansion eines Gases in Vakuum oder Wärmeaustausch zwischen zwei Körpern. |
In Kapitel IX haben wir bereits drei einfache Prozesse, bei denen jeweils eine Variable konstant ist, kennengelernt. Zusätzlich sprachen wir bereits von adiabatischen Zustandsänderungen. Fassen wir noch einmal kurz zusammen:
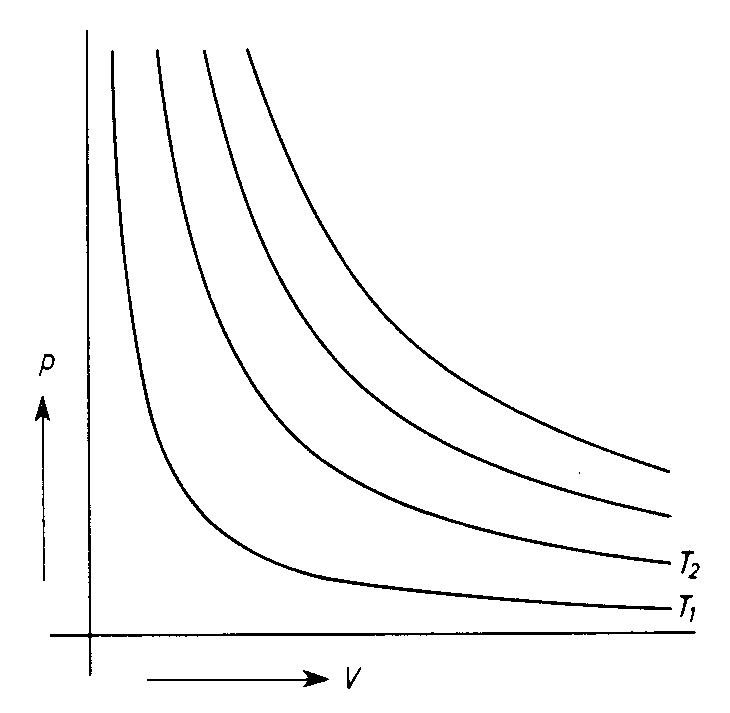
1.
Dann folgt aus
Û ![]()
Û ![]()
Der hyperbelförmige Graph im p/V-Diagramm wird Isotherme genannt.
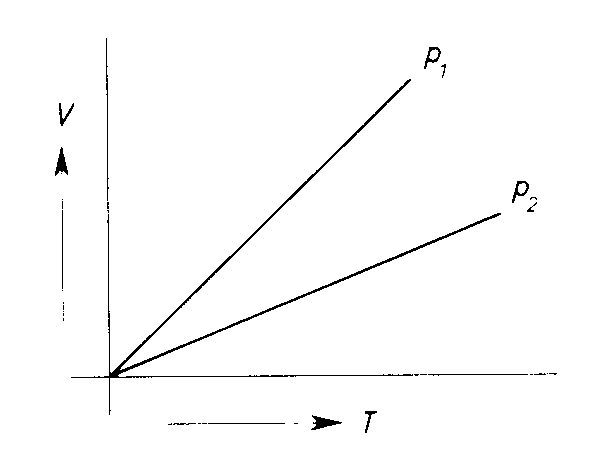
2.
Dann folgt aus
Der lineare Graph im V/T-Diagramm wird Isobare genannt.
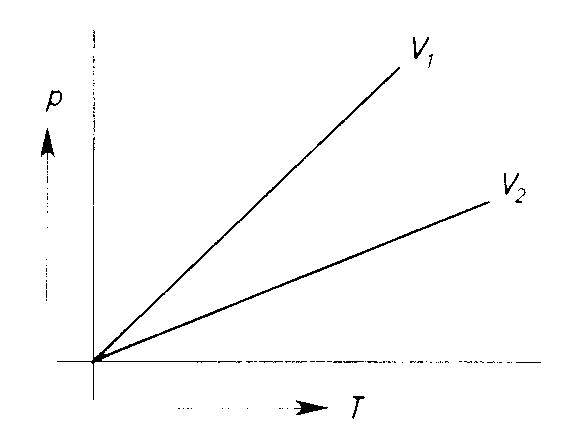
3.
Dann folgt aus
Der lineare Graph im p/T-Diagramm wird Isochore genannt.
4.
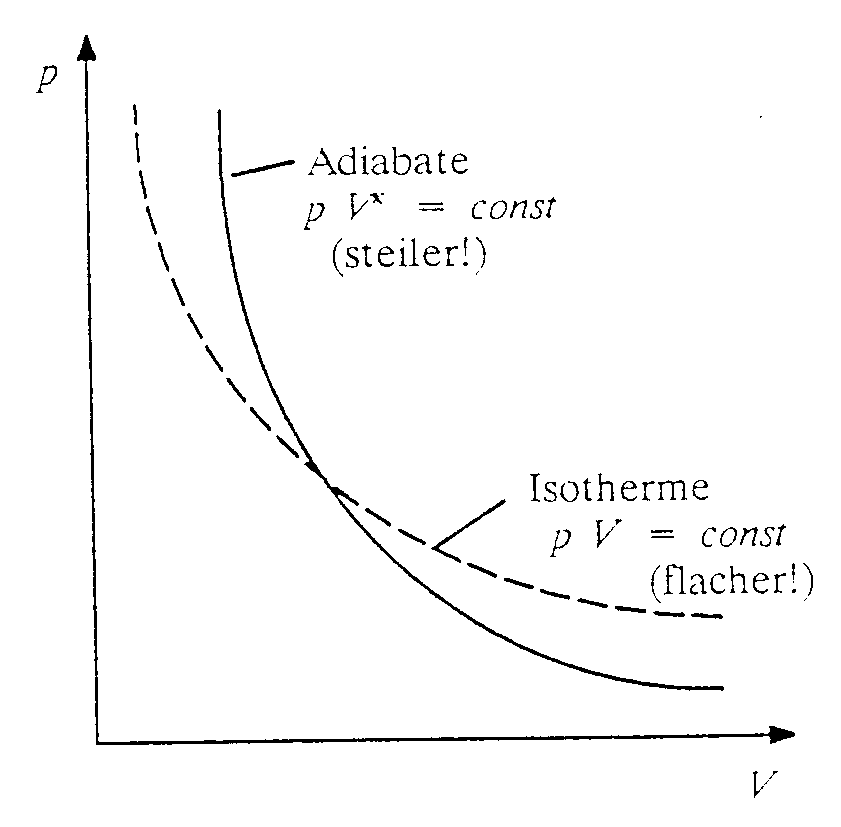
Der hyperbelförmige Graph im p/V-Diagramm wird Adiabate genannt.
T = const. Isotherme Þ dU = 0
V = const. Isochore Þ d W = 0
p = const. Isobare Þ d W = - pdV
Q = const. Adiabate Þ d Q = 0
|
Als Beispiele werden im Folgenden isotherme und adiabatische Zustandsänderung berechnet.
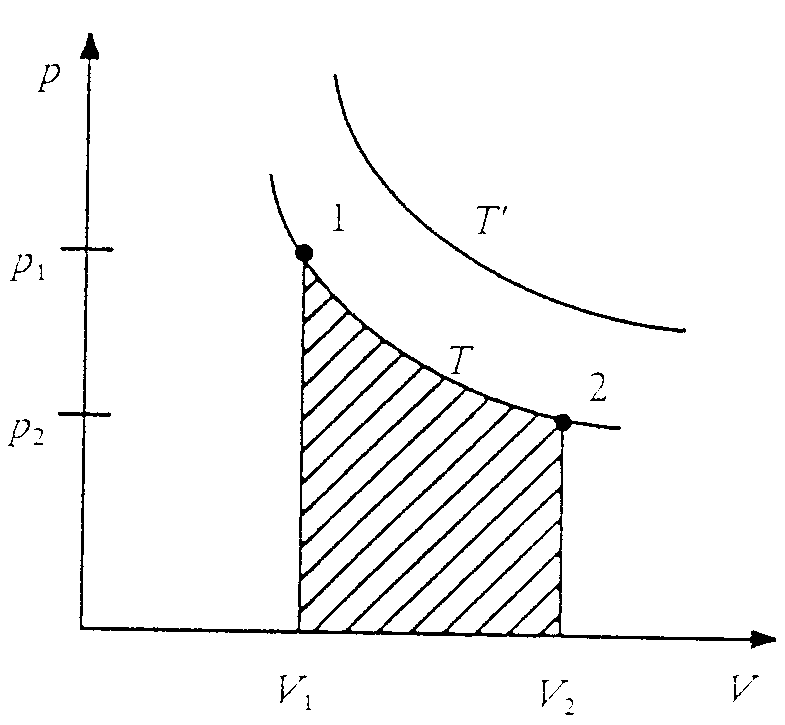 Für isotherme Prozesse gilt
Für isotherme Prozesse gilt
Wegen pV = const sind die Isothermen Hyperbeln.
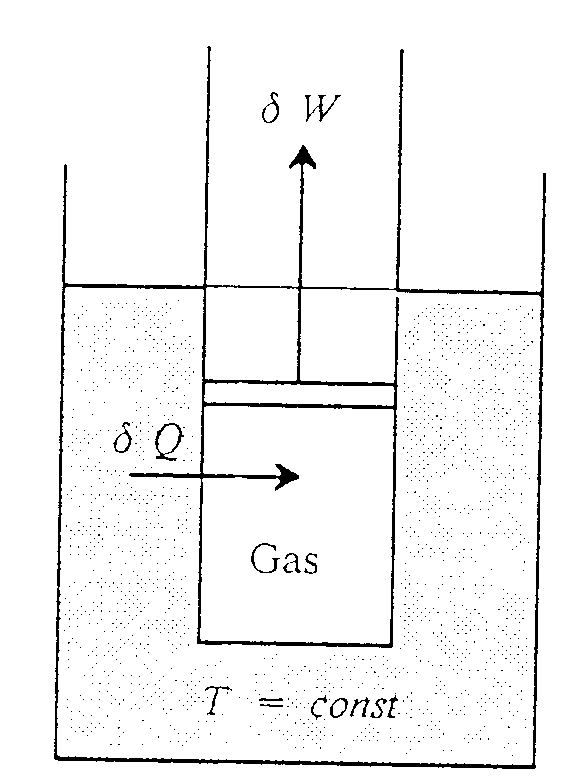
Als Beispiel eines isothermen Prozesses betrachten wir einen Zylinder mit Kolben im Wasserbad. Die Bewegung des Kolbens erfolgt so langsam, daß sich das Gas immer auf der Temperatur des Wasserbades befindet.
Die zugeführte WärmeD Q, die für die Vergrößerung des Volumens benötigt wird, läßt sich mit dem Energiesatz oder dem I. Hauptsatz berechnen:
Aus dem 1. Hauptsatz
folgt mit der Idealgasgleichung
und der kalorischen Zustandsgleichung
Diese Gleichung hatten wir Energiesatz für ideale Gase genannt. Mit T = const. und folglich dT = 0 folgt für isotherme Prozesse
Dann gilt für die gesamte zugeführte Wärme D Q:
Da der Druck p umgekehrt proportional ist zum Volumen V gilt
mit p ~ 1/V
Die zugefürte Wärme D Q erhöht das Volumen und erniedrigt den Druck. Sie wird als Arbeit pdV abgegeben.
und
 Für adiabatische Zustandsänderungen hatten wir festgehalten:
Für adiabatische Zustandsänderungen hatten wir festgehalten:
Hier bedeutet adiabatisch thermisch isoliert.
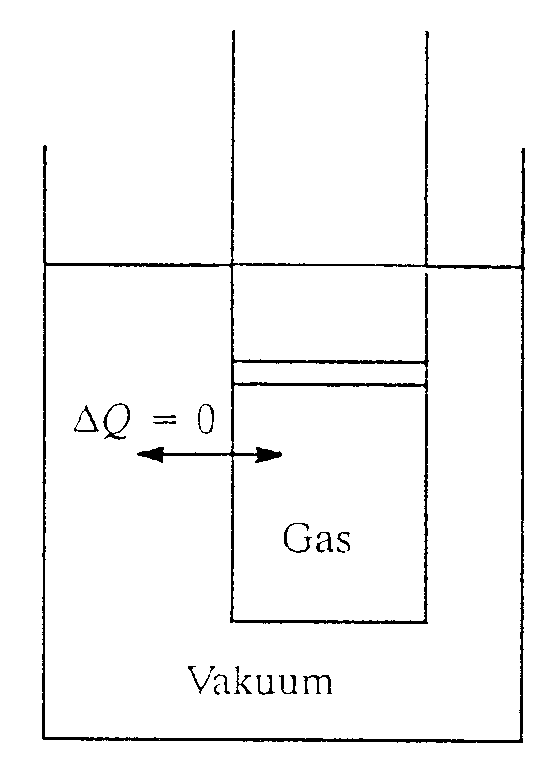
Der Begriff der adiabatischen Zustandsänderung wird häufig auch für Prozesse gebraucht, die beliebig schnell, z.B. Schallwellen, die keine Zeit für Wärmeaustausch mit Umgebung haben, oder hinreichend langsam vor sich gehen, so daß keine Verwirbelungen und damit kein Reibungsverlust entstehen.
Jetzt folgt aus dem Energiesatz:
mit d Q = 0
Für 1 Mol, also n = 1 gilt
Damit folgt aus dem Energiesatz für adiabatische Prozesse
Mit R = CP - CV und k = ![]() gilt
gilt
Damit folgt
Mit T~ p V für ideale Gase gilt dann auch
Diese Gleichung wird Adiabatengleichung genannt. Zur Erinnerung sei noch einmal erwähnt, daß der Adiabatenkoeffizient k immer größer eins ist. Werte von k sind k = 1,667; k = 1,4 usw.
Merke: Für adiabatische Zustandsänderungen gilt die Adiabatengleichung p Vk = const mit k > 1. |
Bei Schallwellen, als Beispiel für adiabatische Zustandsänderung, ergibt sich für die Schallgeschwindigkeit
mit der Gasdichte r. Diese Beziehung kann genutzt werden zur Messung von ![]() .
.
Abschließend betrachten wir einen Versuch:
Versuch XIV.4: Adiabatische und isotherme Zustandsänderung
Bei diesem Versuch wird ein Gasvolumen in einem Glaszylinder mit einem beweglichen Kolben verändert. Auf einer sehr empfindliche Temperaturanzeige kann die momentane Temperatur des Gases abgelesen werden. Zunächst komprimieren wir das Volumen V. Man beobachtet, daß die Temperatur ansteigt.
Wartet man nun bis die Temperatur wieder sinkt, ehe man weiter kompremiert, d.h. bewegt man den Kolben nur sehr langsam, dann pendelt die Temperaturanzeige immer um die Ausgangstemperatur. So kann ein isothermer Prozess nachgewiesen werden.
Bei schneller Bewegung des Kolbens steigt die Temperatur hingegen steil an. Der Wärmeaustausch mit der Umgebung kann so schnell nicht stattfinden, deshalb ist dieser Vorgang adiabatisch.