XIV.4 Enthalpie und Joule-Thomson-Effekt
In diesem Kapitel wird eine neue Zustandsgröße, die Enthalpie, eingeführt. Dieser relativ unbekannte Zustandsgröße wird in Analogie zur inneren Energie U definiert.
Zunächst berechnen wir die Wärme also statt mit CV = const mit CP = const .
Dann gilt
Analog zu U ist damit die gesuchte neue Zustandsgröße definierbar:
Wir setzen mit cP = const für ideales Gas
Die neue Zustandsgröße wird Enthalpie genannt und mit H bezeichnet.
Diese Gleichung heißt 'Gibbsche Wärmefunktion' (q a lp o s = Wärme).
Berechnen wir nun mithilfe dieser Definition die Enthalpie eines Systems:
Es gilt
Erweitern wir nun den ersten Hauptsatz
um V dp - V dp, so folgt
Fassen wir p dV + V dp zusammen zu
so folgt
Mit der Grundannahme p = const folgt
und damit gilt
wegen d Q = dH folgt
Diese Gleichung ist die allgemeine Definition der Zustandsgröße H:
Definition XIV.4: Die Enthalpie H ist definiert als H = U + pV. Die Enthalphie ist eine Zustandsgröße. |
Wie bereits vermutet, ist die Enthalpie eines Stoffes die innere Energie erweitert um die Volumenarbeit, die bei einer Zustandsänderung mit konstantem Druck zusätzlich aufgewandt werden muß.
Für ein ideales Gas ergibt sich
mit U = m cV T und pV = nRT
und mit m cV = CV folgt
Merke: Für ideales Gas berechnet sich die Enthalpie als H = n CpT. |
Bei idealen Gasen bleibt wegen
mit d Q = 0 und d W = 0
also die innere Energie konstant.
Deshalb gilt mit
daß die Temperatur konstant bleibt
 Was passiert bei realen Gasen
Was passiert bei realen Gasen 
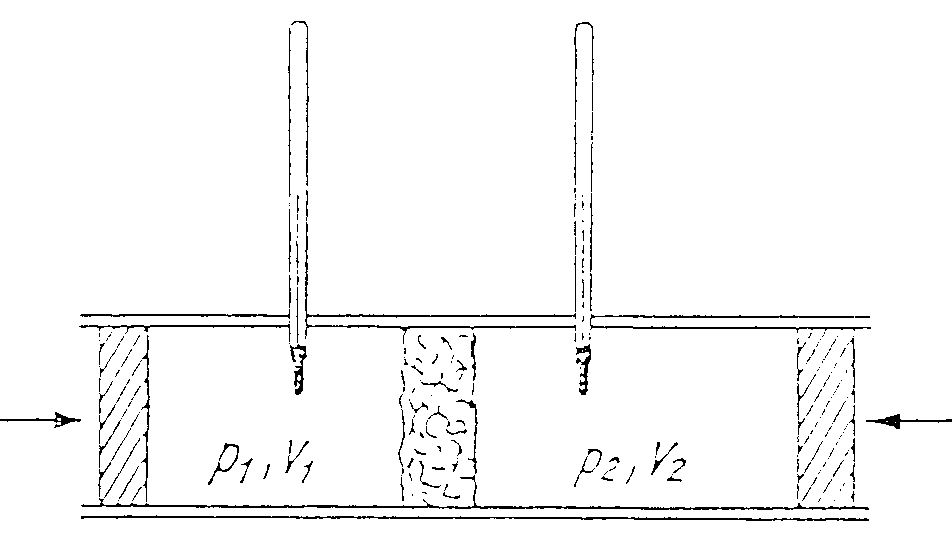
In einem Gedankenexperiment betrachten wir eine gedrosselte Expansion. Dabei tritt der Joule-Thomson-Effekt auf, bei dem ein stationärer Gasstrom aus einem Raum mit konstantem höherem Druck durch eine Drosselstelle, z.B. einen Wattebausch, langsam in einen Raum konstanten niederen Drucks strömt. Zur Vermeidung von Störungen durch Wirbelbildungen des Gases oder zusätzlicher Geschwindigkeit, was eine Erhöhung der kinetischen Energie bedeuten würde, wird dieser Prozeß genügend langsam durchgeführt. Deshalb strömt das Gas langsam durch den Wattebausch. Es wird vorausgesetzt, daß dieser Prozeß adiabatisch, d.h. wärmeisoliert, abläuft. Zur Beantwortung unserer Frage interessieren uns bei diesem Versuch vor allem die Temperaturen vor und hinter der Drosselstelle.
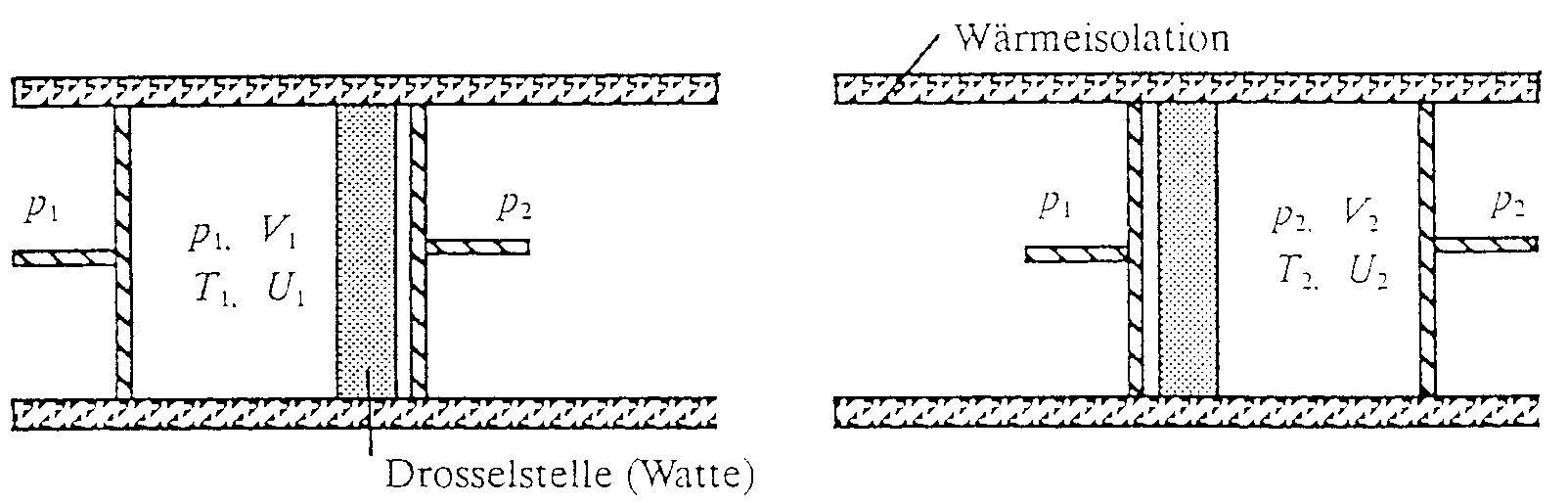
Die bei der Strömung umgesetzte Energie kann man erfassen, indem man sich vorstellt, daß ein bestimmtes Volumen V1 vor der Drosselstelle durch einen Kolben 1 durch diese hindurchgeschoben wird, wobei der Druck p1 konstant gehalten wird. Der Kolben 2 hinter der Drosselstelle wird dann mit dem konstanten Druck p2 vom Gas vor sich hergeschoben. Ist das Gas vollständig durch die Drosselstelle geschoben, nimmt es das Volumen V2 ein.
 Welche Arbeit wird dabei an Volumen 1 geleistet ?
Welche Arbeit wird dabei an Volumen 1 geleistet ?
Für die Expansion des Gases von p1 ® p2 bzw. V1 ® V2 gilt nun
mit
integriert über p = const. gilt
W1 ist die am Volumen 1 geleistete Arbeit.
Anlog gilt mit
integriert über p = const. gilt
W2 ist von Volumen 2 aufgenommene Arbeit. Aufgrund unserer Vorzeichenkonvention ist die aufgenommene Arbeit W2 negativ.
Mit dem 1. Hauptsatz
und
folgt dann dU = d Q + W1 + W2
Þ dU = d Q + p1 V1 - p2 V2
Da der Prozeß adiabatisch verläuft gilt
und damit
Û U2 - U1 = p1 V1 - p2 V2
Û U1 + p1 V1 = U2 + p2 V2
mit H = U + pV folgt
Bei einem idealen Gas mit
oder
Wie bereits berechnet, bleibt bei einem idealen Gas die Temperatur konstant. Dagegen zeigt der Joule-Thomson-Effekt für ein reales Gas, daß die innere Energie nicht nur von der Temperatur abhängig ist, sondern U = U (p,T) oder U = U (V, T) Bei realem Gas bleibt die Enthalpie erhalten. Die Enthalphie als Erhaltungsgröße bei der sogenannten 'isenthalpischen Entspannung' zeigt, daß es sinnvoll ist, eine Größe so zu definieren.
Merke: Bei einer isenthalpischen Entspannung bleibt bei einem idealen Gas die Temperatur, bei einem realen Gas die Enthalpie erhalten. |
Nun müssen wir die Enthalpie H für ein reales Gas bestimen:
Allgemein gilt
Um H zu bestimmen müssen wir also den Druck p und die innere Energie U bestimmen.
Der Zusammenhang zwischen diesen Zustandsgrößen wird durch die Van-der-Waals-Gleichung beschrieben:
Eingesetzt in H = U + pV folgt
Die innere Energie U eines idealen Gases
muß für ein reales Gas erweitert werden um einen Korrekturglied,das aus der Anziehung der Moleküle resultiert. Mit
folgt
Dann folgt für die innere Energie
Eingesetzt in
folgt
Bei einer isenthalpischen Entspannung ist
und folglich
Um die erste Ableitung dieser Gleichung zu berechnen, führen wir den Begriff der totalen Differentials ein:
Definition XIV.5: Totales oder vollständiges Differential einer Funktion f von zwei Variablen an der Stelle (x0, y0) nennt man den Ausdruck |
Bildet man nun das totale Differential dH erhält man:
Durch Lösung dieser Gleichung findet man zwei Möglichkeiten:
1. Abkühlung:
![]()
falls
2. Erwärmung
falls
Tinv ergibt sich durch Lösen der Gleichung. Für ![]() ergibt sich nämlich der Term
ergibt sich nämlich der Term
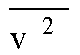
Man bezeichnet ![]() mit m, dann gilt
mit m, dann gilt
m
wird als Joule-Thomson-Koeffizient bezeichnet.Die Einheit des Joule-Thomson-Koeffizienten ist [ m ] = K/105 Pa
Definition XIV.6: Die Inversionstemperatur ist durch m = 0 definiert: Tinv = |
Experimentell wird dieser Wert auf 10 ¸ 30 % bestätigt.
Für jedes Gas gibt es eine bestimmte Inversionstemperatur Tinv mit der Eigenschaft, daß sich bei
Die Inversionstemperatur Tinv gibt an, wann bei einer Druckänderung, d.h. einer Abstandsänderung der Moleküle, abstoßende oder anziehende Kräfte überwiegen. Einmal wird die Temperatur und die kinetische Energie erhöht, im anderen Fall erniedrigt.
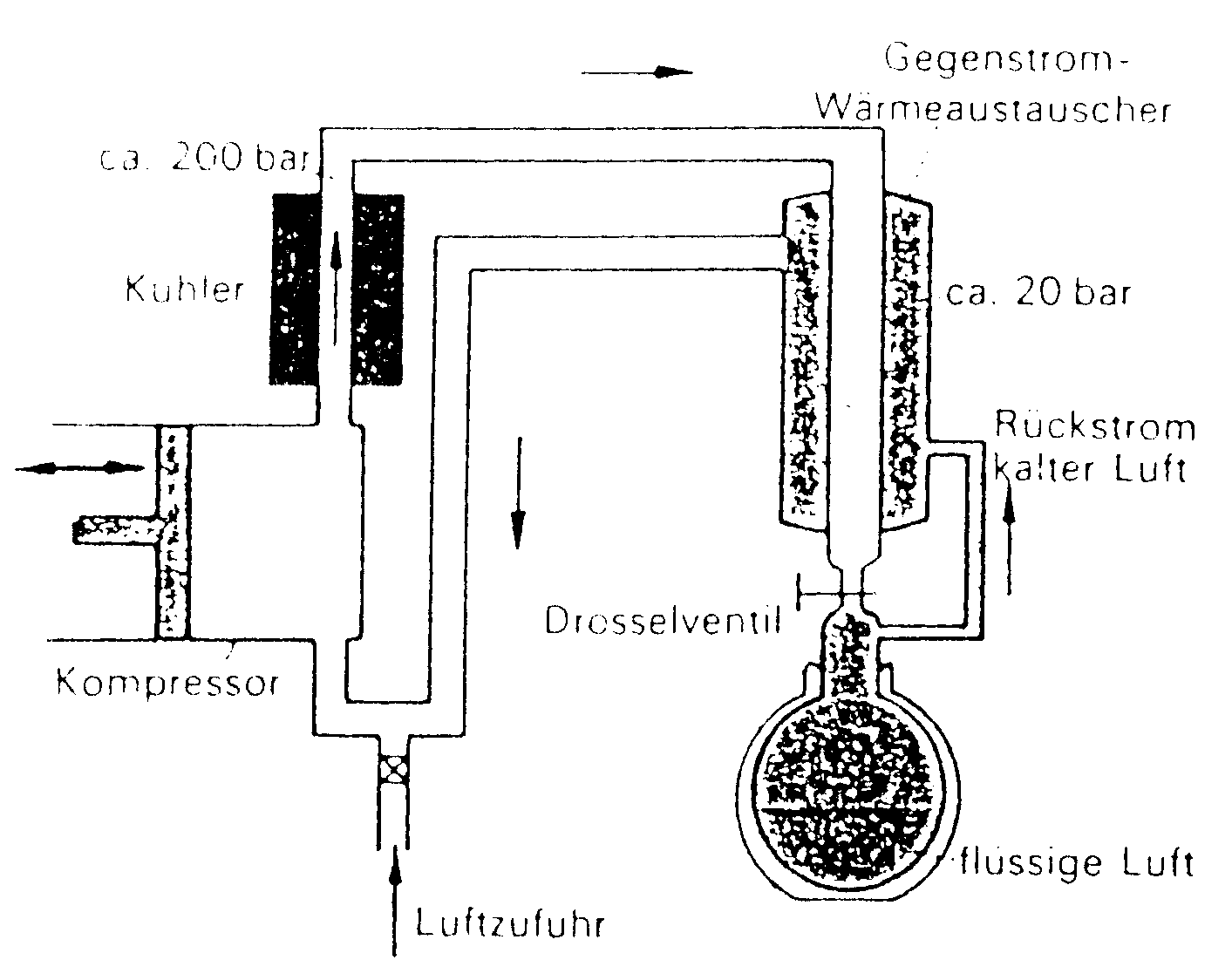
Im Verfahren von Linde wird z.B. der Joule-Thomson-Effekt zur Verflüssigung von Gasen ausgenutzt. Hier wird mittels Kompression Arbeit in das Gas gesteckt und durch einen Kreislauf werden ausreichend niedrige Temperaturen erreicht.
Anschaulich wird die obige Rechnung für Spezialfälle:
1) Die Gasmoleküle besitzen kein Eigenvolumen, es wirken nur Anziehungskräfte. Gegen diese Anziehungskräfte muß Arbeit geleistet werden, die Temperatur sinkt.
Rechnerisch zeigt sich mit
ist aufgrund der Anziehung
Für großes V2
wegen
2) Im zweiten Fall werden die Anziehungskräfte vernachlässigt, die Eigenvolumina hingegen nicht. Realisierbar ist dieser Fall z.B. mit Edelgas
Mit
folgt wegen des Kovolumens
wegen
Die Änderung der Temperatur eines Gases wollen wir in einem kleinen Versuch demonstrieren:
Versuch XIV.3: Schnee im Hörsaal
Bei diesem Versuch wird eine Flache mit CO2 auf Zimmertemperatur aufgedreht. Durch eine kleine Öffnung entweicht das Gas. Dabei sinkt die Temperatur des Gases hinter der Drosselstele so weit ab, daß Schnee entsteht.
Wasserstoff kann erst durch Vorkühlen unterhalb Tinv verflüssigt werden.
Das bedeutet aber auch, daß Wasserstoff sich bei einem Leck bei Zimmertemperatur erhitzen kann. Hier besteht Explosionsgefahr !