XIV.3 Spezifische Wärme idealer Gase
Wir hatten definiert, daß die Proportionalitätskonstante zwischen Wärmemenge d Q und Temperaturänderung dT einer Masse m spezifische Wärme genannt wird:
Der Quotient aus Wärmemenged Q und dem Produkt aus Temperaturänderung dT und der Masse m des erwärmten Körpers wird spezifische Wärme c genannt:
|
Die Einheit der spezifischen Wärme ist
Im allgemeinen Fall verändert sich bei der Zustandsänderung eines idealen Gases sowohl sein Volumen als auch der Druck. Diese Fälle sind schwer zu berechnen. Einfacher hingegen berechnet man die innere Energie idealer Gase, wenn eine der beiden Größe Druck oder Volumen konstant bleiben. Diese beiden Fälle untersuchen wir nun genauer:
Um zu verdeutlichen, daß diese Rechnung nur für konstante Volumen gilt, wird die spezifische Wärme mit dem Index V gekennzeichnet: spezifische Wärme cV.
Dann schreiben wir für die spezifische Wärme
Es gilt der 1. Hauptsatz
und mit d W = - p dV folgt
Mit der Grundannahme, das Volumen sei konstant, also dV = 0 folgt dann
In ¼ eingesetzt ergibt
Im Einklang mit der kinetischen Gastheorie steht die Annahme, die spezifische Wärme cv konstant ist. Die innere Energie U ist proportional zur Temperatur T: U = U(T). Daraus folgt direkt, daß cv konstant ist:
Aus
folgt durch Integration
Bezeichnen wir die innere Energie des Gases im Anfangszustand mit U0 und die Temperaturdifferenz mit T, so gilt die 'kalorische Zustandsgleichung'
Als wichtigstes Ergebnis ist festzuhalten, daß die innere Energie des idealen Gases linear mit der Temperatur ansteigt. Die unbestimmte Konstante Uo ist aufzufassen als der Teil der inneren Energie, der bei thermodynamischen Prozessen keine Rolle spielt. Mit Hilfe der Thermodynamik können über Uo keine Aussagen gemacht werden. Da jedoch zwischen zwei Zuständen nur Energieunterschiede auftreten, ist es möglich Uo = 0 zu wählen. Diese Wahl vereinfacht die kalorische Zustandsgleichung auf die Form
Merke: Die kalorische Zustandsgleichung idealer Gase lautet
U = m cV T mit Uo= 0 |
Aus dem 1. Hauptsatz
folgt mit der Idealgasgleichung
und der kalorischen Zustandsgleichung
Diese Gleichung wird Energiesatz für ideale Gase genannt:
Merke: Der Energiesatz für ideale Gase lautet:
d Q = m cV dT + |
Wie bereits in Kapitel X eingeführt, wird bei Gasen oft nicht die Masse m betrachtet sondern die Anzahl der Teilchen, also die molaren Größen. Deshalb definieren wir die molare Wärmekapazität bezogen auf ein Mol:
Definition XIV.2: Die Molwärme oder molare Wärmekapazität CV wird definiert als
CV |
Die Einheit der molaren Wärme ist
Betrachten wir nun den 2. Fall:
Analog zu dem ersten Fall bezeichnen wir die spezifische Wärme bei konstantem Druck mit cp.
Die Zustandsänderung eines Gases mit gleichbleibenden Druck muß andere Auswirkungen haben, als die bei konstantem Volumen: Zusätzlich zur Erwärmung muß nun auch Ausdehnungsarbeit geleistet werden. Zur Berechnung betrachten wir ein Gedankenexperiment:
Gas wird erhitzt, dehnt sich dabei aus und leistet Arbeit.
Zunächst gilt der 1. Hauptsatz
Nach unserer Vorzeichenkonvention gilt damit
mit p = const.
Mit der Definition der molaren Wärmekapazität angewandt auf konstanten Druck
![]() =
= ![]()
folgt
bezogen auf ein Mol schreiben wir mit Vm = ![]() als Volumen pro Mol und Um =
als Volumen pro Mol und Um = ![]() als innere Energie pro Mol
als innere Energie pro Mol
Der Term ![]() ist bereits aus dem 1. Fall bekannt. Er bezeichnet die molare Wärmekapazität bei konstantem Volumen, also
ist bereits aus dem 1. Fall bekannt. Er bezeichnet die molare Wärmekapazität bei konstantem Volumen, also
Nun müssen wir versuchen, den zweiten Term ![]() zu interpretieren. Hierfür betrachten wir noch einmal die Idealgasgleichung
zu interpretieren. Hierfür betrachten wir noch einmal die Idealgasgleichung
Die Ableitung der Idealgasgleichung für ein Mol
nach T ergibt:
Mit der Kettenregel gilt
Für p = constant gilt schließlich
Damit folgt aus ¼
![]()
Merke: Für molare Wärmekapazität bei konstantem Volumen und konstantem Druck gilt das Verhältnis
|
Diese Gleichung zeigt, daß die molare Wärmekapazität bei konstantem Druck größer ist als bei konstantem Volumen. Dieses Ergebnis ist aufgrund der Ausdehnungsarbeit anschaulich verständlich.
Merke: Für die Molwärme gilt: |
Um diese Frage zu beantworten, müssen wir die innere Energie U kennen. Aus Kapitel XIV.2 wissen wir, daß für ein ideales Gas, d.h. Moleküle ohne Ausdehnung, gilt ![]() .
.
Dabei gingen wir davon aus, daß ideale Gasmoleküle Punktmassen sind und deshalb nur drei Freiheitsgrade der Translation besitzen. In Kapitel XI hatten wir den Begriff der Freiheitsgrade eingeführt:
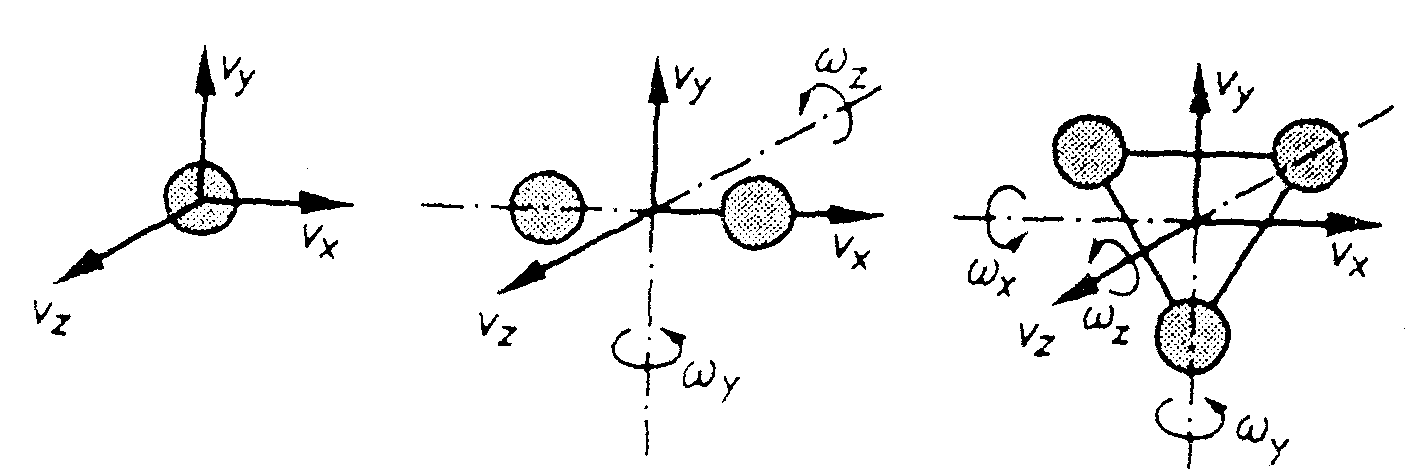
Wir hatten in der kinetischen Gastheorie festgestellt, daß bei der regellosen Bewegung eines Gasmoleküls keine Raumrichtung bevorzugt wird. Deshalb besitzt jedes Teilchen entsprechend den drei räumlichen Richtungen drei voneinander unabhängige Bewegungsmöglichkeiten. Wie definierten den Ausdruck jedes Teilchen besitzt drei Freiheitsgrade der Translation.
Besteht das Molekül nicht nur aus einem Atom, so hat es zusätzlich die Bewegungsfreiheit, sich um bestimmte Achsen zu drehen. Ein solches Molekül kann zusätzlich drei Freiheitsgrade der Rotation besitzen, je nachdem, ob die Drehachse raumfest ist (1 Freiheitsgrad) oder ob sie sich in einer Ebene bewegen kann (2 Freiheitsgrade) bzw. ob die Drehachse frei im Raum beweglich ist. Diese Überlegung zu einem späteren Zeitpunkt in der Experimentalphysik vertieft.
Allgemein hatten wir die innere Energie U eingeführt als mittlere kinetische Energie aller Gasmoleküle:
mit der Anzahl f der Freiheitsgrade gilt allgemein für 1 Mol
Die innere Energie pro mol Um ist die Summe aus der mittleren kinetischen Energie von NA Molekülen, also
Die mittlere kinetische Energie eines Moleküls berechnet man nach Kapitel X als
Dann gilt
Mit NA k = R folgt
Aus der Gleichung
folgt durch Differentation
Aus ![]() folgt
folgt
Merke: Für die Molwärme idealer Gase gilt
CV = |
Das Verhältnis von Molwärme bei konstantem Volumen und bei konstantem Druck berechnet sich dann als
Da ![]() ist, ist dieses Verhältnis immer größer 1. Man nennt dieses Verhältnis Adiabatenkoeffizient.
ist, ist dieses Verhältnis immer größer 1. Man nennt dieses Verhältnis Adiabatenkoeffizient.
Definition XIV.3: Der Adiabatenkoeffizient k ist das Verhältnis der Molwärme bei konstantem Druck zur Molwärme bei konstantem Volumen:
|
Im Bezug auf die Anzahl der Freiheitsgrade f unterscheidet man vier Fälle:
1. 1-atomige Gase
Beispiele für 1-atomige Gase sind die Edelgase Helium (He), Neon (Ne), Argon (Ar), aber auch Natrium- oder Quecksilber-Dampf (Na- oder Hg-Dampf)
Diese Gase haben wie bereits erläutert nur 3 Translationsrichtungen und damit drei Freiheitsgrade
Dann gilt
Der Aiabatenkoeffizient k ist
Merke: Für 1-atomige Gase gilt CV = |
2. 2-atomige Gase
Hier können als Beispiele H2, N2, O2 oder HCl aufgezählt werden.
Beschrieben werden diese Moleküle durch ein mechanisches Modell, das sogenannte Hantelmodell. Eine Hantel kann sich in drei Raumrichtungen bewegen, hat also 3 Freiheitsgrade der Translation.
Bei mehratomigen Molekülen muß man zudem Freiheitsgrade der Rotation betrachten: Das Molekül kann bei einer frei im Raum beweglichen Drehachse zusätzlich drei Freiheitsgrade der Rotation besitzen. Bei linearen Molekülen, zu denen z.B. die zweiatomigen Moleküle gehören, fällt bei Energiebetrachtungen ein Freiheitsgrad weg: Das Trägheitsmoment bezüglich der Hantelachse ist ebenso vernachlässigbar wie bei einatomigen Gasen. Die Energie, die nötig wäre um ein Atom um diese Achse in Rotation zu versetzen ist folglich so groß, daß sie nicht eintritt.
Merke: Für lineare, speziell 2-atomige Gase gilt: CV = |
3. 3-atomige Gase
Beispiele hierfür sind H20-Dampf oder NH3 . Bei diesen Atomen können alle drei Rotationsrichtungen angeregt werden. Deshalb besitzen sie
Merke: Für 3-atomige Gase gilt: CV = 3R, CP = 4R und k = |
4. Schwingung
Bei höheren Temperaturen sind Schwingungen der Atome gegeneinander möglich. Mit Schwingung ist die Zahl der Freiheitsgrade für ein zweiatomiges Gas f = 7. Der Schwingung entsprechen zwei Freiheitsgrade, da im Mittel die Hälfte der Energie in potentieller, die andere Hälfte in kinetischer Energie steckt. Für die Temperatur ist nur die kinetische Energie entscheidend, aber diese kann nicht erhöht werden, ohne daß auch die potentielle Energie erhöht wird.
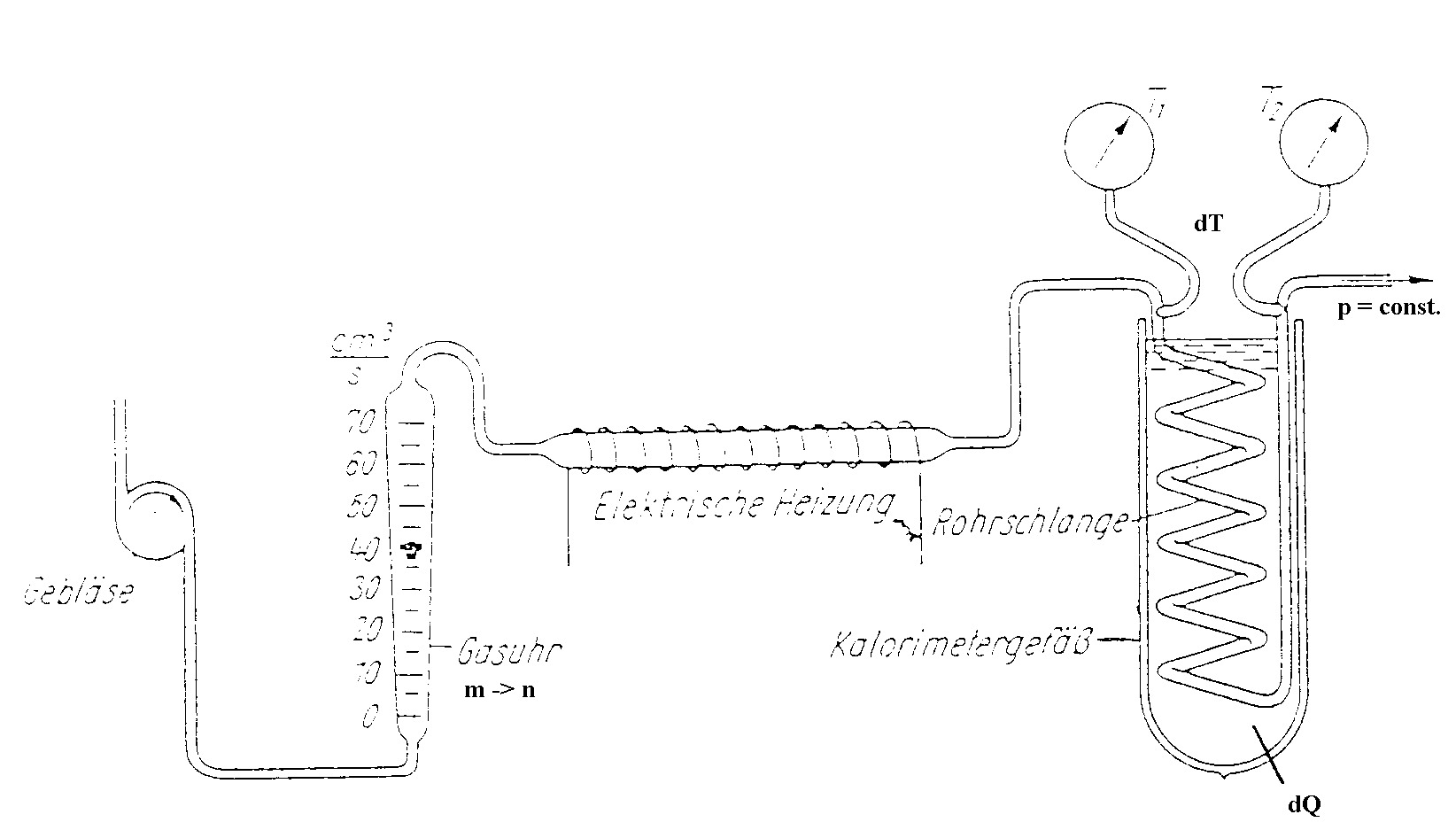
Ein Verfahren zur Bestimmung der molaren Wärmekapazitäten ist der Versuch nach Pohl:
CP läßt sich im strömenden Gas mit einem Versuch nach Pohl messen, indem man es erhitzt und durch eine Rohrwendel in ein Kalorimeter fließen läßt. Aus der Temperaturdifferenz, aus der durchflossenen Gasmenge und aus der im Kalorimeter abgegebenen Energie wird die Molwärme CP bestimmt. Die Berechnung ergibt die Formel
Da dieser Versuch für die Vorlesung zu kompliziert ist, wollen wir einen anderen Versuch zeigen:
Versuch XIV.2: Bestimmung des Adiabatenkoeffizienten
Bei diesem Versuch wird ein Glaskolben mit Gas gefüllt und anschließend mit einem frei beweglichen Stopfen verschlossen. Im Ruhezustand wird die Stellung des Stopfens markiert. Sie werde mit x bezeichnet und sei x = 0. Drückt der Stopfen nun mit seiner Masse m auf das Gasvolumen, so wird das Gas komprimiert. Es entsteht ein Druck, der den Stopfen zurücktreibt über die Ruhelage hinaus. So entsteht ein Unterdruck und Kolben wird wieder nach unten gedrückt. Die so entstehende Schwingung ist leider durch Reibung des Stopfens am Glaskolben gedämpft. Um diese Dämpfung zu umgehen, wird der Stopfen periodisch durch einen Gasstrom angetrieben. So entsteht eine erzwungene Schwingung mit gleichbleibender Amplitude.
Bevor wir die Schwingungsgleichung aufstellen und mit Hilfe der Kenntnisse aus der Mechanik lösen, muß kurz ein neuer Begriff eingeführt werden:
Wir hatten in Kapitel XI den Begriff der Isothermen kennengelernt. Die Isothermen (T = const.) sind im p/V-Diagramm als Hyperbeln darstellbar. Es galt
Analog zu den Isothermen nennt man die Kurven im p/V - Diagramm ohne Wärmeaustausch (d Q = 0) Adiabaten. Aufgrund einer Gleichung, die wir später herleiten werden,
sind diese Hyperbeln steiler als die Isothermen.
Mit Kenntnis dieser neuen Gleichung können wir die Schwingungsgleichung aufstellen:
Auf den Korken wird die Kraft
Diese Kraft erzeugt einen Druck mit
mit der Grundfläche A des Korkens. Die Druckdifferenz ist für positive Volumenänderungen negativ, denn die Kraft wirkt der Volumenvergrößerung entgegen.
Mithilfe der neuen Gleichung pVk = constant können wir dp berechnen.
Es gilt
Dann folgt aus
mit dV = Ax gilt
Aus dieser Schwingungsgleichung kann man die Winkelgeschwindigkeit ablesen:
mit ![]() .
.
Durch Messen der Frequenz kann man den Adiabatenkoeffizient bestimmen, da m, p, r und V durch den Versuchsaufbau vorgegeben sind.
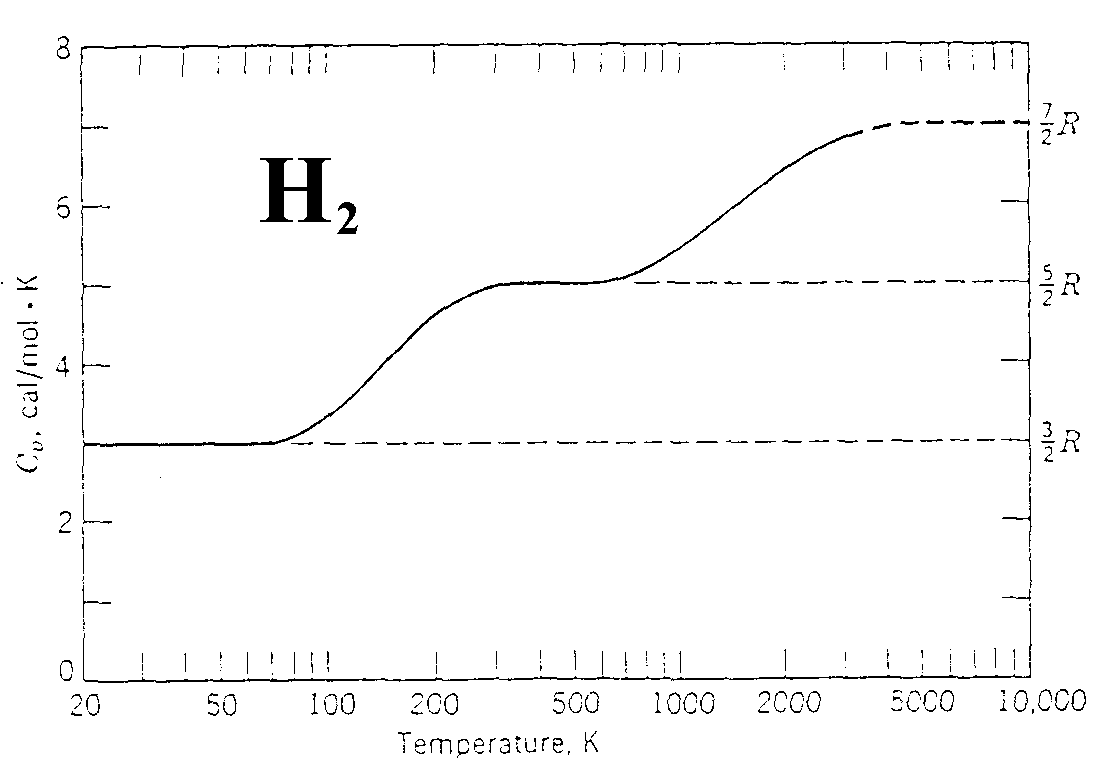
Variation of the molar heat Cr of hydrogen with temerature. Note that T is drawn on a logarithmic scale. Hydrogen dissociates before 3200 K is reached. The dashed curve is for a diatomic molecule that does not dissociate before 10.000 K is reached.
Eine