XIV.2 Innere Energie von Gasen
Bei einem Gas sind die Zustandsgrößen U, p, V, T sind nicht unabhängig voneinander, im allgemeinen ist U = U (p, V, T) z.B. für ein reales Gas. Die innere Energie ist die Summe aller in einem System (Gas, Festkörper,...) enthaltenen Energien (potentielle und kinetische Energie).
Der Sonderfall, den wir behandeln wollen ist das ideale Gas. Laut Definition gibt es in einem idealen Gas keine Anziehungskräfte, also keine potentielle Energie, sondern nur kinetische Energie.
Um die innere Energie idealer Gase genauer zu untersuchen, überlegte J. Gay Lussac (1778 - 1850) sich einem Versuch. Diesen Versuch wollen wir als Gedankenexperiment nachvollziehen und auswerten:
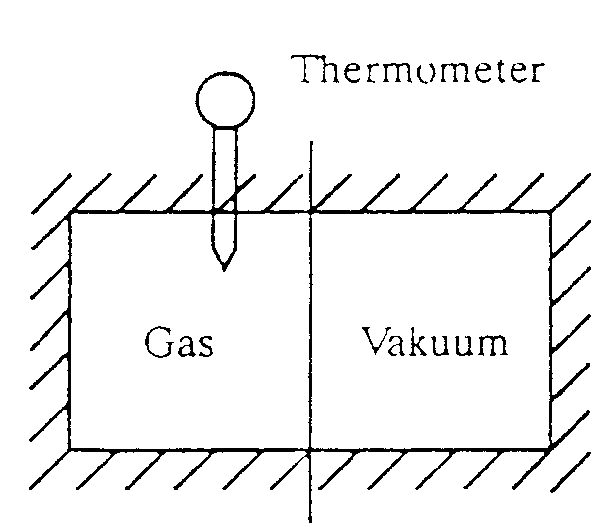
Lussac untersuchte die freie Expansion eines idealen Gases. Bei dem Versuch wird ein thermisch isoliertes Gefäß durch eine Trennwand geteilt. Das Gas befindet sich in einem Teilraum, in dem anderen Teilraum sei Vakuum. Der Zustand des Gases wird gemessen, im Speziellen wird mit einem Thermometer die Temperatur des Gases bestimmt.
Danach wird die Trennwand entfernt. Das Gas kann sich jetzt im gesamten Volumen ausbreiten. Mißt man nach einiger Zeit, wenn sich ein Gleichgewicht eingestellt hat, erneut die Temperatur, so kann man keinen Unterschied zu der ursprünglichen Temperatur finden.
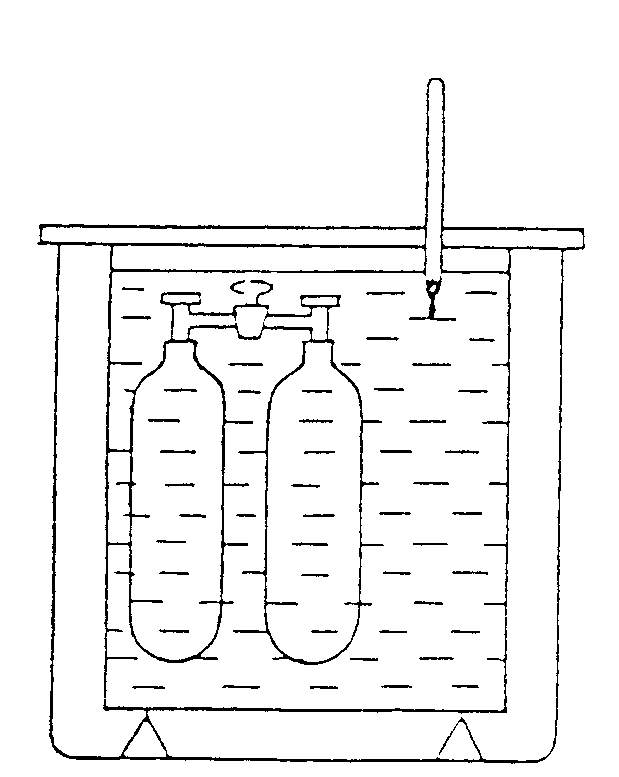
Aus dem vorherigen Kapitel wissen wir, daß die Änderung der inneren Energie zwischen den beiden Zuständen
ist. Da bei dem Versuch eine freie Expansion erfolgt ist, d.h. keine Arbeit aufgewendet wurde, gilt
Das Gefäß soll thermisch isoliert sein, es kann dann weder Wärme nach außen gelangen noch von außen in das Volumen eindringen:
Damit gilt für die innere Energie
Bei diesem Versuch wurde damit ein eindeutiger Zusammenhang zwischen der inneren Energie U und der Temperatur T hergeleitet
Zusammenfassend können wir schreiben:
Merke: In einem idealen Gas hängt die innere Energie nur von T ab: U = U(T). |
Die Erklärung aus der kinetischen Gastheorie greift auf die eingangs zusammengefaßten Formeln
zurück:
Der Energieinhalt eines idealen Gases wird durch kinetische Energie der Moleküle bestimmt:
Für ein Mol eines idealen Gases gilt daher
Merke: Für ideale Gase ist die innere Energie
U = |
Und entsprechend gilt für n Mol:
Der Übergang zum realen Gas ist schwieriger.
Generell könnte U bei realen Gasen von allen anderen Zustandsgrößen abhängig sein.
Die innere Energie ist dann eine Funktion von zwei Zustandsgrößen, da die Gasgleichung für reale Gase die drei Variablen verbindet:
Merke: Für reale Gase ist die innere Energie eine Funktion zwei anderer Zustandsgrößen
U ş U (p, V); (p, T); (V, T) |
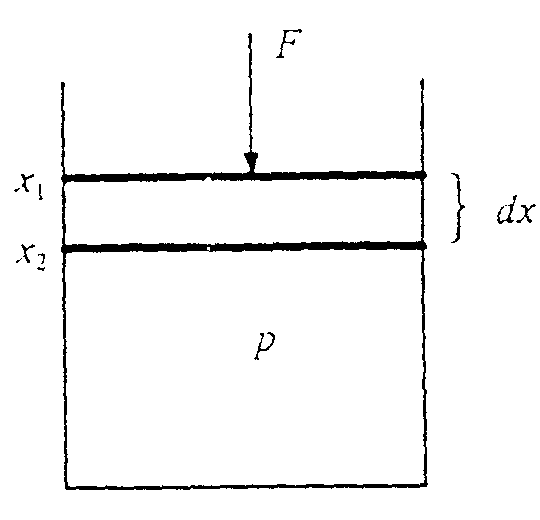
Nun wollen wir ein Beispiel betrachten für die Änderung innerer Energie eines Systems durch mechanische Arbeit. Hierzu betrachten wir erneut ein Gedankenexperiment:
Ein Gasvolumen V sei in einem zylinderförmigen Gefäß mit konstantem Druck p und einer Temperatur T. Durch einen beweglichen Stempel, der um eine Strecke dx nach unten verschoben wird, werde dieses Volumen nun verringert.
Allgemein kennen wir aus der Mechanik die Definition der Arbeit als Produkt aus zurückgelegtem Weg und dafür benötigter Kraft
Nach der Definition des Drucks als Kraft pro Fläche wird durch diese Kraft F auf die Fläche A des Stempels ein Druck ausgeübt, so daß gilt
Das veränderte Volumen berechnet sich aus Grundfläche A mal Höhe dx. Dann folgt für die mechanische Arbeit
Nach unserer Vorzeichenkonvention wurde das Vorzeichen so gewählt, daß die am System geleistete Arbeit, also die zugeführte Energie positiv wird. Arbeit wird dem System zugeführt, wenn das Volumen verkleinert wird, d.h. D V = A (x2 - x1) = V2 - V1 negativ ist. Dann ist die Arbeit d W positiv. Falls sich das Gas ausdehnt, also Arbeit nach außen abgibt, ist die Volumenänderung dV positiv und d W = - p dV ist negativ, wie vereinbart.
Als nächstes Beispiel betrachten wir einen Kreisprozeß:
Die Berechnung der Arbeit für eine Änderung des Volumens von V1 auf V2 auf dem Weg a erfolgt durch das Integral:
Aus der Analysis ist bekannt, daß ein solches Integral die Fläche angibt, die der Graph im p/V-Diagramm mit der Abszisse einschließt.
Verändert man das Volumen anschließend auf einem beliebigen Weg von V2 nach V1, so muß dafür die Arbeit
aufgewandt werden. Es ist offensichtlich
Dann gilt
Im allgemeinen aber gilt diese Beziehung nicht, also
Im pV-Diagramm ist in diesem Fall die Differenz der Arbeit d W die Fläche zwischen den Kurven von Punkt 1 nach Punkt 2 und zurück. Die gesamte Arbeit bei diesem Kreisprozeß die von den beiden Kurven (a,b) eingeschlossene Fläche. Obwohl wir zum Anfangszustand (1) zurückkehren, kann ![]() sein. Das zeigt noch einmal, daß die Arbeit vom Weg abhängt und keine Zustandsgröße ist.
sein. Das zeigt noch einmal, daß die Arbeit vom Weg abhängt und keine Zustandsgröße ist. ![]() ist dagegen, wie wir wissen, immer gleich Null.
ist dagegen, wie wir wissen, immer gleich Null.