XIV.1 I. Hauptsatz der Thermodynamik
Dieser Satz ist nach der mechanischen Deutung der Wärme durch die kinetische Gastheorie fast selbstverständlich. Als Ausgangslage der statistischen Mechanik hatten wir bereits postuliert, daß Wärme eine andere Form der Energie sein muß.
Der zweite Teil des Hauptsatzes ist für alle Bereiche der Physik über die Mechanik und die Thermodynamik heraus gültig:
Die Gesamtenergie eines abgeschlossenen Systems ist erhalten.
Das gilt für alle uns bisher bekannten mechanischen Energien, für Wärme und für noch nicht besprochene Energien, z.B. Gravitationsenergie als Verallgemeinerung der potentiellen Energie, elektromagnetische Energie, insbesondere auch chemische Energie, Kernenergie und andere.
Eine grundlegende Erweiterung des ersten Hauptsatzes fand noch einmal durch A. Einstein statt, der in seiner viel zitierten Formel E = mc2 festhielt, daß auch die Masse nur eine andere Form von Energie ist. Damit wurden erneut zwei bis dahin als getrennt angesehene Erhaltungssätze verknüpft:
Der Erhaltungssatz für Energie Eund der
Erhaltungssatz für Masse m
Masse ist eine andere Form der Energie.
Anschaulich ist der erste Hauptsatz der Wärmelehre also klar. Nun müssen wir versuchen, diesen Satz auch quantitativ zu konkretisieren.
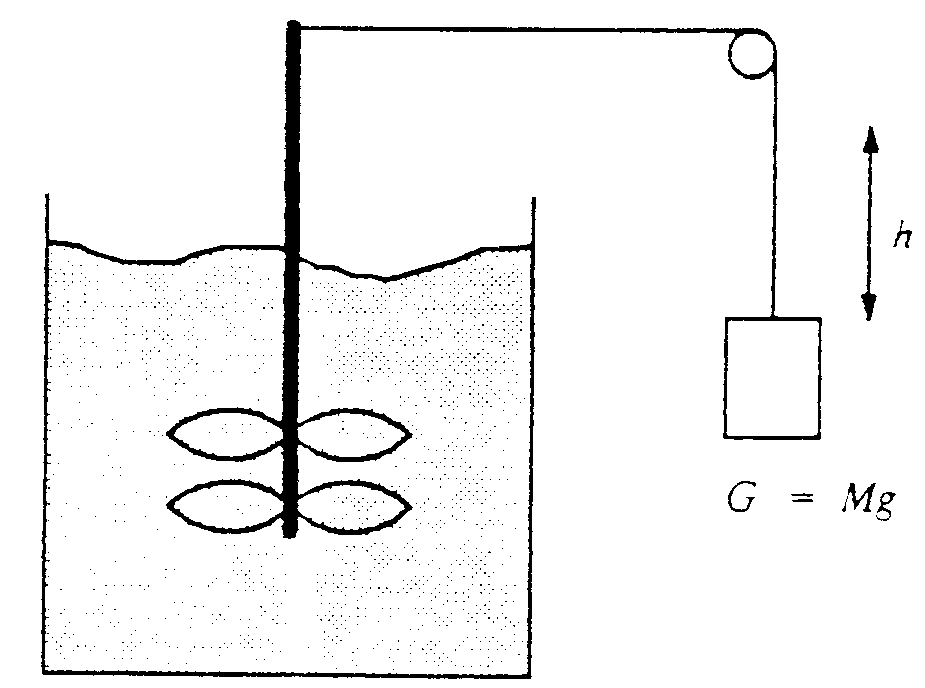
Die Umwandlung von Wärmeenergie in mechanische Arbeit wurde in einem einfachen Versuch nachgewiesen:
Über eine Umlenkrolle wird ein Gewicht M mit einem Seil an einem Rührwerk befestigt. Das Rührwerk mit großer Reibung wird über die Gewichtskraft G angetrieben, die auf die Masse M wirkt, sobald man das Gewicht fallen läßt. Zunächst beweist die Bewegung des Rührwerkes, daß eine Umwandlung existiert: Zudem kann man mit diesem historischen Versuch den Umrechnungsfaktor der mechanischen Arbeit in Wärme berechnen:
Fällt die Masse m um eine Höhendifferenz h, so wird an ihr die Arbeit
Durch die Reibung des Rührwerks in dem Wasser wird das Wasser erhitzt. Eine Temperaturdifferenz von D T bedeutet bei Wasser der Masse m eine Wärmeänderung von
Die Umwandlung von W nach Q kann aus diesen beiden Beziehungen berechnet werden.
Einen ähnlichen Versuch wollen wir in der Vorlesung betrachten:
Versuch XIV.1: mechanisches Wärmeäqivalent
In diesem Versuch wird statt des Wärmebads eine Kupferscheibe erwärmt. Dazu wird eine Kupferscheibe zwischen Bremsbelägen und einem Thermoelement eingespannt. Nun wird über eine Umlenkrolle mittels eines fallenden Gewichts die Kupferscheibe gegen die Bremsbeläge in Rotation versetzt. Durch die so entstehende Reibungsenergie erwärmt sich das Kupfer. Das Thermoelement mißt diese Temperaturänderung und gibt sie direkt an ein Computerauswertungsprogramm weiter.Mit einer am Seil hängenden Masse von M = 10 kg, einer Fallhöhe von h = 1 m, der spezifischen Wärmekapazität von Kupfer cCu = 0,092 cal/g × K und der Masse der angetriebenen Kupferscheibe von m = 150 g ergibt die Messung eine Temperaturänderung D T = 1.7 K.
Das Verhältnis von geleisteter Arbeit und erzeugter Wärme ist damit D W/D Q = 4.18 J/cal.
Versuche mit anderen Materialien und variiertem Versuchsaufbau zeigen, daß dieser Umwandlungsfaktor konstant ist. Er wird mechanisches Wärmeäquivalent genannt. Der Theoriewert beträgt:
Mechanisches Wärmeäquivalent:
D W/D Q = 4.185 J/cal |
Aufgrund der allgemeinen Proportionalität von Q und W ist es empfehlenswert, beide Größen in einer Einheit anzugeben. Man einigte sich auf die Konvention, beide Größen in Nm, also in Joule, anzugeben.
Mit dem mechanischem Wärmeäquivalent als Umrechnung gilt dann
Merke: In einem abgeschlossenen System gilt DW = D Q mit dem mechanischem Wärmeäquivalent als Umrechnung. |
Jetzt haben wir gesehen und bewiesen, daß Wärme eine andere Form von Energie ist. In den früheren Kapiteln hingegen haben wir Wärme beschrieben durch Zusammenhänge, z.B. das Idealgasgesetz pV = nRT, mit anderen Größen. Was aber haben nun die anderen Größen aus der Wärmelehre, also Druck p, Volumen V und Temperatur T mit dieser Form der Energie zu tun ?
Um diese Frage mathematisch beantworten zu können, reflektieren wir noch einmal den Charakter dieser Größen:
p, V, T sind Zustandsgrößen: Diese Größen sind unabhängig von der Vorgeschichte eines Systems eindeutig meßbar. Sie beschreiben also den Zustand eines Systems zu einer festen Zeit.
Merke: Zustandsgrößen sind Größen die unabhängig von der Vorgeschichte eines Systems eindeutig meßbar sind. |
Die in einem System gespeicherte Wärmemenge hingegen ist keine Zustandsgröße: Eindeutig meßbar ist nur die Temperaturänderung eines Systems, und diese muß nicht ausschließlich durch Zuführen von Wärme erzeugt werden, sondern kann z.B. durch Kompression erzielt werden.
Wir unterscheiden im Folgenden Zustandsgrößen und andere Größen. Um nun die Zustandsgrößen und die anderen Größen unterscheiden zu können, wird eine neue Schreibweise benutzt:
Notation XIV.1: Auml;nderung von Zustandsgrößen: dp, dT, dV, dU,... Auml;nderung anderer Größen: d W, d Q,... |
Bevor wir neue Zusammenhänge für die Energie eines Systems herleiten, sind hier noch einmal stichwortartig die wichtigsten Ergebnisse über die Energie eines Systems aus den vorherigen Kapiteln zusammengestellt:
Durch die Zurückführung der Gesetze auf Mechanik hatten wir in der kinetischen Gastheorie folgende Gesetze festgehalten:
Ziel dieser Überlegungen ist es, eine Zustandsgröße zu finden, die anders als die Wärme oder Arbeit den Zustand eines Systems charakterisiert.
Um den Begriff der 'inneren Energie' verständlich zu machen, betrachten wir zunächst ein abgeschlossenes System. Ein solches System kann realisiert werden durch z.B. ein Gas- oder Flüssigkeitsvolumen. Das System befinde sich zu einer festen Zeit in einem Zustand 1. Dann werde diesem System Energie zugeführt. Das ist möglich entweder durch Leisten mechanischer Arbeit, Zuführen von Wärme oder einer Kombination von beidem. Dieser Vorgang ist dann z.B. das Aufheizen eines Gasvolumens mit gleichzeitiger Kompression. Im Zustand 2 hat das System nun eine andere Energie:
Zur Beschreibung der Zustände führen wir die innere Energie U ein. Dabei wird die Änderung folgendermaßen definiert:
Definition XIV.1 |
Bei dieser Definition muß eine wichtige Vorzeichenkonvention beachtet werden:
Merke: zugeführte Energie (Arbeit oder Wärme) ist positiv,
abgegebene Energie (Arbeit oder Wärme) ist negativ. |
In vielen Büchern wird eine andere Vorzeichenkonvention gemacht und dU = dQ - dW geschrieben. Dann ist dW die vom System geleistete, d.h. abgegebene Arbeit.
Wie können wir Definition XIV.1 anwenden, um eine Formulierung des 1. Hauptsatzes zu bekommen, mit der wir konkret rechnen können ?
Zunächst betrachten wir hierfür den Übergang eines Systems vom Zustand 1 in einen anderen Zustand 2 in Abhängigkeit der bekannten Zustandsgrößen. Im p/V-Diagramm beispielsweise kann ein solcher Übergang so aussehen:
bild fehltNach der Ausführung eines beliebigen Prozesses, bei dem Anfangs- und Endzustand eines Arbeitsstoffes gleich sind, z.B. einem Kreisprozess im p/V-Diagramm, sind definitionsgemäß p, V und T gleich. Ohne weitere Zusatzkenntnisse können über die geleistete Arbeit W oder die zugeführte Wärme Q jedoch keine Aussagen gemacht werden.
Da nach dem ersten Hauptsatz jedoch D W und D Q äquivalent sind, führt die Summe immer zum gleichen Ergebnis D U.
Die Innere Energie U ist also anders als die Wärme Q oder die Arbeit W eine Zustandsgröße. Damit haben wir eine Größe definiert, die unabhängig von den vorherigen Änderungen eines Systems jederzeit bestimmt werden kann. Mit einer solchen Zustandsgröße können wir Systeme charakterisieren.
Die Änderung der Inneren Energie D U = U(2) - U(1) ist nur vom Anfangs- und Endzustand abhängig und nicht vom 'Weg', d.h. von der Art, wie die Innere Energie verändert wurde.
Mathematisch können wir diese Größen, die unabhängig vom Weg sind, schreiben als
Merke: Die innere Energie U ist eine Zustandsgröße, so daß gilt: |
Merke: Mit d U = (d Q + d W) gilt für die Summe der Nicht-Zustandsgrößen Wärme und Arbeit |
Aus diesen Sätzen ergeben sich zwei neue Formulierungen des 1. Hauptsatzes:
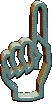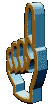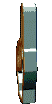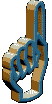
Äquivalent ist die Aussage, daß die Summe aus zugeführter Wärme und geleisteter Arbeit null sein muß, wird das System in einen Endzustand gleicher innerer Energie transferiert. Das bedeutet, daß man kein System erzeugen kann, welches Arbeit leistet ohne die entsprechende Menge Wärme aufzunehmen. Eine solche Maschine wird Perpetuum mobile 1. Art genannt.
Diese zweite Formulierung des Hauptsatzes sagt nicht notwendig, daß die Änderung der Wärme null sein muß (![]() ) und keine Wärme aufgenommen oder abgegeben werden darf (
) und keine Wärme aufgenommen oder abgegeben werden darf (![]() ). Wärme und Arbeit sind keine Zustandsgrößen es sind vielmehr Formen in denen Energie transportiert werden kann.
). Wärme und Arbeit sind keine Zustandsgrößen es sind vielmehr Formen in denen Energie transportiert werden kann.