

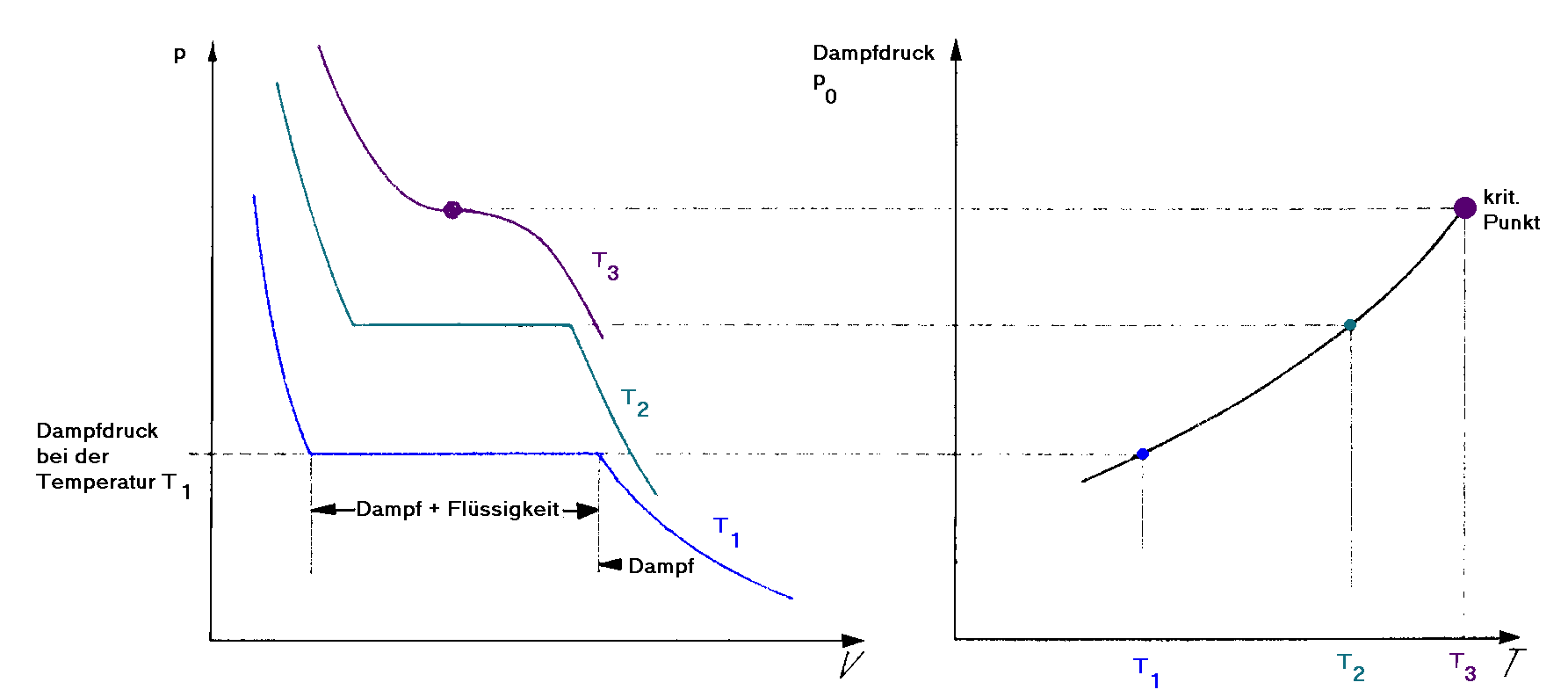
Merke: Die Dampfdruckkurve im p/T-Diagramm gibt p(T) an, bei dem die flüssige und die gasförmige Phase koexistieren. |
 Will man eine Dampfdruckkurve messen, so braucht man dazu nur einen geschlossenen Behälter, der teilweise mit Wasser gefüllt ist. Heißt man dieses Wasser nun auf und mißt Temperatur und Druck, so erhält man die Dampfdruckkurve.
Wir wollen einen etwas anderen Versuch vorführen:
Will man eine Dampfdruckkurve messen, so braucht man dazu nur einen geschlossenen Behälter, der teilweise mit Wasser gefüllt ist. Heißt man dieses Wasser nun auf und mißt Temperatur und Druck, so erhält man die Dampfdruckkurve.
Wir wollen einen etwas anderen Versuch vorführen:
Versuch XII.1: Aufnahme der Dampfdruckkurve
Wir füllen einen geschlossenen Behälter mit Schwefelhexachlorid und Quecksilber. Der Behälter ist so konstruiert, daß wir das Volumen verringern können; zudem wird der Druck im Innnern des Gefäßes gemessen. Zuerst verringern wir das Volumen des Gases, wie zu erwarten steigt der Druck an. Ab einem bestimmten Druck bildet sich plötzlich eine Flüssigkeitsoberfläche. Verringert man nun das Volumen, so bleibt der Druck konstant, während die Flüssigkeitsoberfläche sich vergrößert. Im p/V- Diagramm befinden wir uns jetzt auf der Maxwellgraden. Der konstante Druck ist der Dampfdruck. Erst wenn das Gas ganz verflüssigt ist, erhöht sich dfer Druck bei weiterer Volumenverringerung. Die so aufgenommenen Kurve läßt sich durch Volumenverringerung und der daraus resultierenden Verdampfung wieder zurückfahren. In einem zweiten Versuch soll gezeigt werden, daß man den oben skizzierten Verlauf auf der van der Waals-Kurve teilweise auch über die Maxwell-Grade hinaus realisieren kann.Versuch XII.2: Verzug beim Erstarren
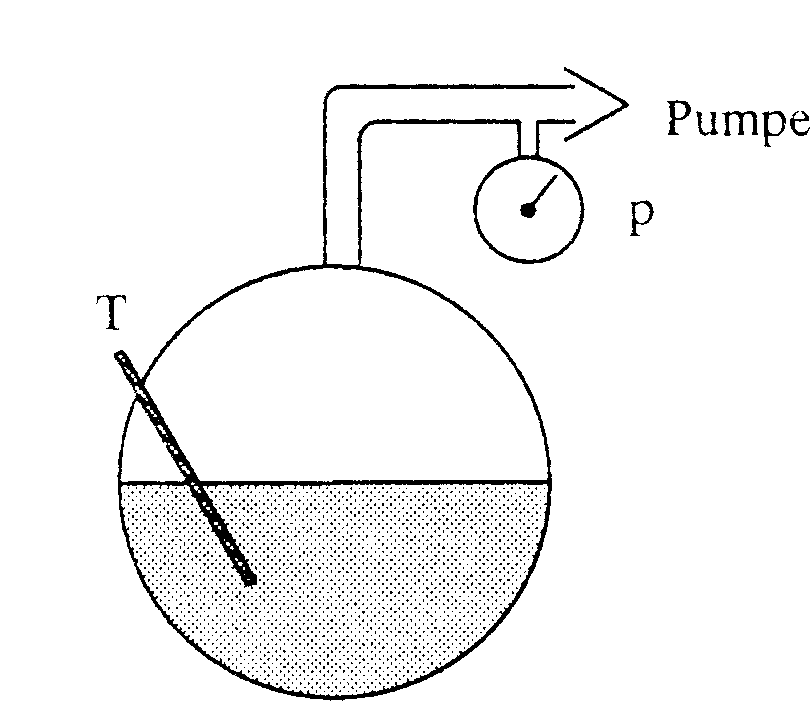 Für diese Demonstration wird ein Gefäß mit Wasser teilweise aufgefüllt. Über eine Pumpe kann die darüber befindliche Luft abgesaugt und so der Druck verringert werden. Die durch Verringerung des Drucks sinkende Temperatur des Wassers wird gemessen.
Zunächst können wir beobachten, daß wie erwartet bei Verringerung des Drucks die Temperatur sinkt. Spannend wird der Versuch ab einer Temperatur von knapp 0°C. Bei dieser Temperatur erwarten wir eigentlich, daß das Wasser anfängt zu gefrieren. Bei unserem Versuch können wir die Temperatur jedoch bis auf -4°C herunterfahren, ohne daß das Wasser erstarrt. Offensichtlich folgen wir in diesem Bereich der van der Waals-Graden statt der korrigierenden Maxwell-Graden. Schüttelt man nun aber am Gefäß, so schlägt der Aggregatzustand schlagartig um und das Wasser erstarrt vollständig. Jetzt sind wir wieder auf die Maxwellgrade zurückgesprungen. Wie vorhergesagt liegt die Temperatur des Eises bei 0°C.
Für diese Demonstration wird ein Gefäß mit Wasser teilweise aufgefüllt. Über eine Pumpe kann die darüber befindliche Luft abgesaugt und so der Druck verringert werden. Die durch Verringerung des Drucks sinkende Temperatur des Wassers wird gemessen.
Zunächst können wir beobachten, daß wie erwartet bei Verringerung des Drucks die Temperatur sinkt. Spannend wird der Versuch ab einer Temperatur von knapp 0°C. Bei dieser Temperatur erwarten wir eigentlich, daß das Wasser anfängt zu gefrieren. Bei unserem Versuch können wir die Temperatur jedoch bis auf -4°C herunterfahren, ohne daß das Wasser erstarrt. Offensichtlich folgen wir in diesem Bereich der van der Waals-Graden statt der korrigierenden Maxwell-Graden. Schüttelt man nun aber am Gefäß, so schlägt der Aggregatzustand schlagartig um und das Wasser erstarrt vollständig. Jetzt sind wir wieder auf die Maxwellgrade zurückgesprungen. Wie vorhergesagt liegt die Temperatur des Eises bei 0°C.
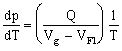
Diese Gleichung der Dampfdruckkurve wird Gleichung von Clausius-Clapeyron genannt.
Merke: Die Dampfdruckkurve wird beschrieben durch die Gleichung von Clausius-Clapeyron
|
Merke: Die Schmelzkurve wird beschrieben durch die Gleichung von Clausius-Clapeyron |
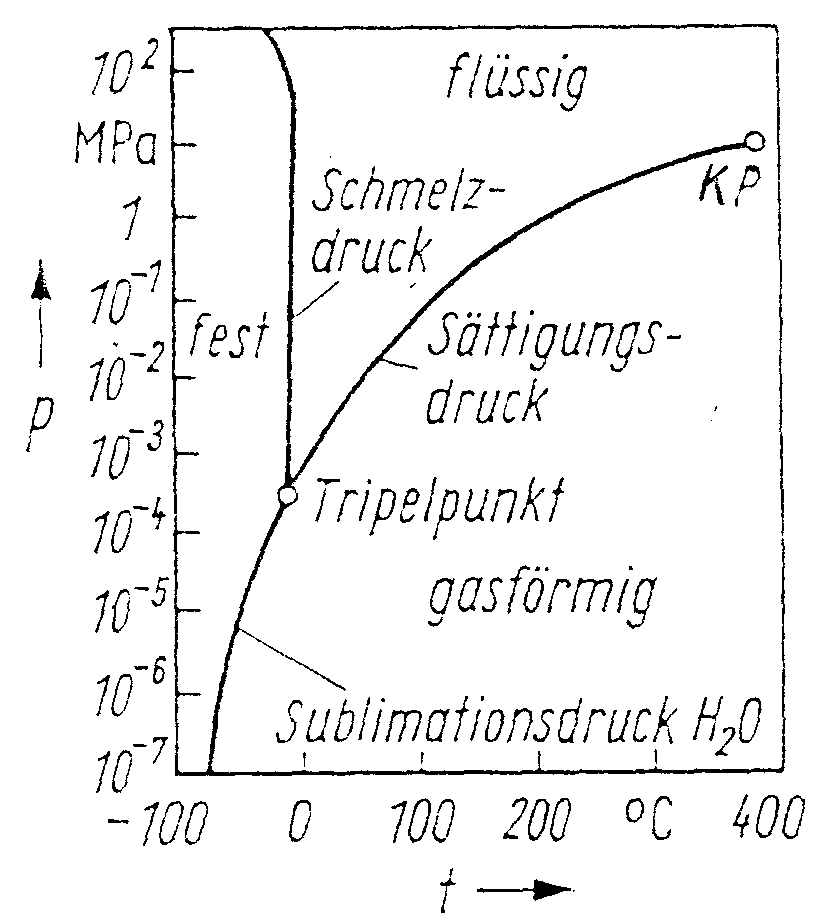 Im Allgemeinen die Änderung des Drucks mit der Temperatur
Im Allgemeinen die Änderung des Drucks mit der Temperatur Versuch XII.3: Süffi
 Süffi ist ein Vogel aus Glas. Er besteht aus einem kugelförmigen Bauch, in dem ein dünner, zu beiden Seiten offener Glaszylinder endet. Am oberen Ende des Glaszylinderhalses sitzt der Kopf, ein kleineres rundes Gefäß, welches direkt mit dem Hals verbunden ist. Vorne am Kopf befindet sich der Schnabel, ein kleines offenes Röhrchen mit Filz überzogen. Der Bauch von Süffi wird soweit mit Wasser gefüllt, daß bei aufrechtem Stand die im Bauch befindliche Halsöffnung im Wasser steht. Bringt man den Vogel in Nähe eines Wassertroges und tippt ihn leicht aus der Gleichgewichtslage an, so neigt er sich immer mehr dem Wasser zu, nimmt schließlich wippend ein paar Schluck und wippt dann wieder höher ohne zu trinken. Bekommt er von dieser Bewegung wieder Durst, beugt er sich mit jedem Wippen weiter runter und trinkt wieder.
Die Erklärung ist folgende:
Durch die Berührung des Schnabels mit gekühltem Wasser zieht sich das Gasvolumen in Süffis Körper zusammen und die Flüssigkeit dehnt sich aus. Der Vogel bekommt Übergewicht und kippt soweit nach vorne, daß das Röhrchen in seinem Bauch nicht mehr im Wasser ist. Das Wasser läuft aus dem Röhrchen, das Gewicht des Kopfes wird kleiner und der Vogel schnellt zurück. Dieses System basiert auf der Temperaturdifferenz zwischen Kopf, der gekühlt wird, und Schwanz, der Zimmertemperatur hat. Deshalb ist diese Bewegung kein perpetuum mobile, also keine Bewegung die endlos läuft ohne Energie zugeführt zu bekommen. Die Energie wird gewonnen aus der Temperaturdifferenz.
Man erzählt sich, daß frühere Kulturen diese Erklärung noch nicht kannten und deshalb einen Riesensüffi als Gott anbeteten, weil er Maschinen zum Laufen bringen konnte, wenn man ihm ein Wasseropfer darbrachte. Entmytologisiert fristet Süffi heute ein Dasein in Physiksammlungen.
Süffi ist ein Vogel aus Glas. Er besteht aus einem kugelförmigen Bauch, in dem ein dünner, zu beiden Seiten offener Glaszylinder endet. Am oberen Ende des Glaszylinderhalses sitzt der Kopf, ein kleineres rundes Gefäß, welches direkt mit dem Hals verbunden ist. Vorne am Kopf befindet sich der Schnabel, ein kleines offenes Röhrchen mit Filz überzogen. Der Bauch von Süffi wird soweit mit Wasser gefüllt, daß bei aufrechtem Stand die im Bauch befindliche Halsöffnung im Wasser steht. Bringt man den Vogel in Nähe eines Wassertroges und tippt ihn leicht aus der Gleichgewichtslage an, so neigt er sich immer mehr dem Wasser zu, nimmt schließlich wippend ein paar Schluck und wippt dann wieder höher ohne zu trinken. Bekommt er von dieser Bewegung wieder Durst, beugt er sich mit jedem Wippen weiter runter und trinkt wieder.
Die Erklärung ist folgende:
Durch die Berührung des Schnabels mit gekühltem Wasser zieht sich das Gasvolumen in Süffis Körper zusammen und die Flüssigkeit dehnt sich aus. Der Vogel bekommt Übergewicht und kippt soweit nach vorne, daß das Röhrchen in seinem Bauch nicht mehr im Wasser ist. Das Wasser läuft aus dem Röhrchen, das Gewicht des Kopfes wird kleiner und der Vogel schnellt zurück. Dieses System basiert auf der Temperaturdifferenz zwischen Kopf, der gekühlt wird, und Schwanz, der Zimmertemperatur hat. Deshalb ist diese Bewegung kein perpetuum mobile, also keine Bewegung die endlos läuft ohne Energie zugeführt zu bekommen. Die Energie wird gewonnen aus der Temperaturdifferenz.
Man erzählt sich, daß frühere Kulturen diese Erklärung noch nicht kannten und deshalb einen Riesensüffi als Gott anbeteten, weil er Maschinen zum Laufen bringen konnte, wenn man ihm ein Wasseropfer darbrachte. Entmytologisiert fristet Süffi heute ein Dasein in Physiksammlungen.