Grundlage bei der Betrachtung idealer Gase war die Idealgasgleichung.
 Wie ändert sich diese Gleichung unter Berücksichtigung der Ausdehnung von Molekülen und der zwischenmolekularen Kräfte?
Wie ändert sich diese Gleichung unter Berücksichtigung der Ausdehnung von Molekülen und der zwischenmolekularen Kräfte?
1) Betrachten wir zunächst die Folgen des Eigenvolumens der Moleküle. Die Tatsache, daß wir eine solches Eigenvolumen nicht unwesentliche Effekte hervorruft, haben wir bereits bei Versuch XI. akzeptiert. Hier haben wir bei unserem Modell nur die Volumendifferenz des Gases in ruhendem und 'geschütteltem' Zustand als Rechnungsgrundlage genutzt. Das Eigenvolumen der Moleküle steht für Bewegungen nicht zur Verfügung. Bezeichnen wir das wegen des Eigenvolumen der Moleküle in einem mol Gas nicht für Bewegungen zur Verfügung stehende Volumen mit b, so bleibt als Restvolumen
das Volumen b wird Kovolumen genannt.
Dieses Kovolumen entspricht nicht dem Eigenvolumen der Gasmoleküle:
 Ein Molekül mit dem Radius r hat ein Volumen von
Ein Molekül mit dem Radius r hat ein Volumen von
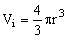
.
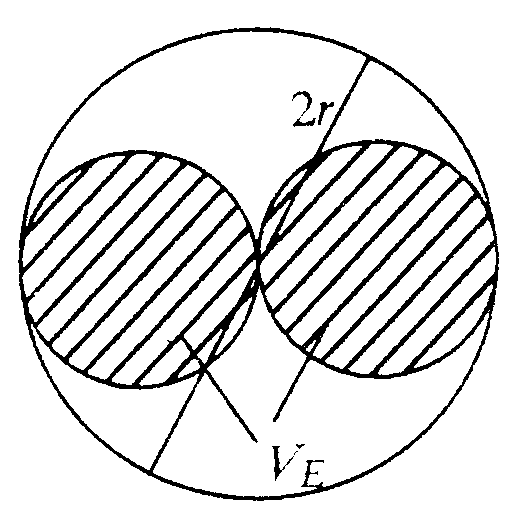
Wie die Abbildung XII.1 zeigt, können sich zwei Moleküle eines realen Gases aber nur auf den Abstand 2r nähern, bis sie zusammenstoßen. Dem einen Molekülmittelpunkt ist der Raum einer Kugel vom Radius 2r gesperrt. Das bedeutet eine Volumenminderung pro Molekül von
Das bedeutet eine Volumendifferenz im Vergleich zum Zusammenstoß zweier Punktmassen von
Das Kovolumen b entspricht also dem vierfachen Eigenvolumen VE der Moleküle. In einem mol muß deshalb insgesamt das Kovolumen
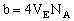
.
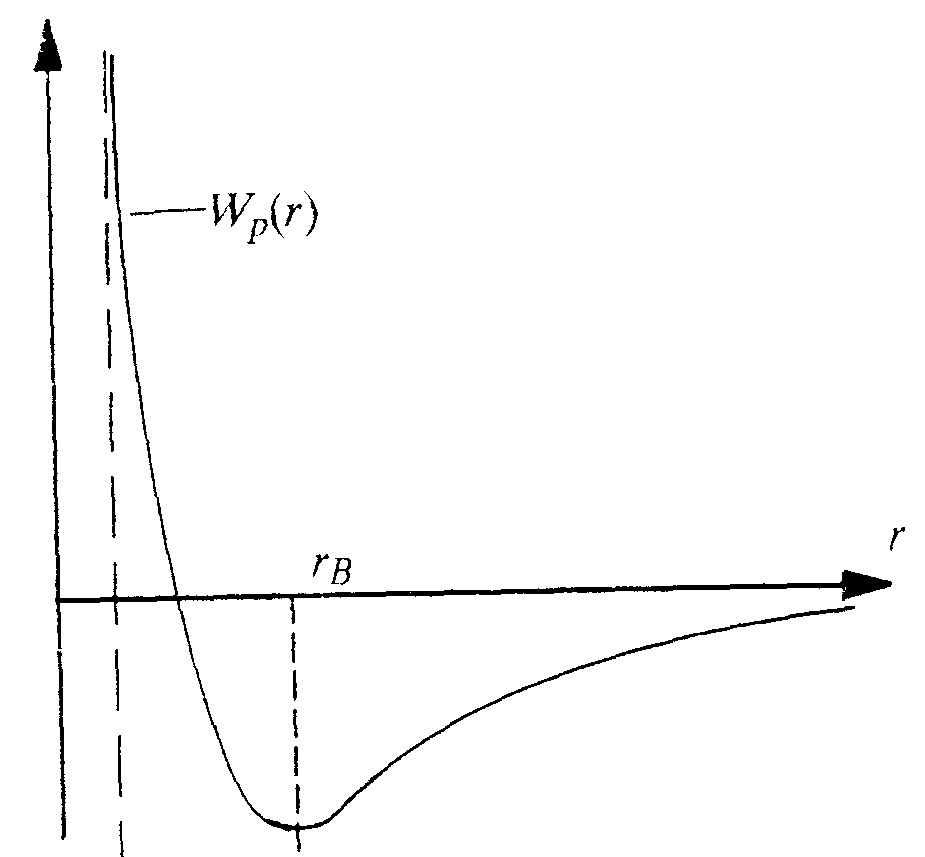 Das Diagramm, in dem die potentielle Energie eines Moleküls in Abhängigkeit von der Entfernung zu einem zweiten Molekül aufgetragen ist, zeigt, daß die potentielle Energie in der direkten Nähe eines zweiten sehr groß ist. Die potentielle Energie ist im Bindungszustand an niedrigs-ten, der Abstand der Moleküle im Bindungszustand sei rB. Entfernt sich das Molekül weiter, so wird die Anziehungskraft der Moleküle schnell kleiner und konvergiert schließlich gegen null.
Diese Anziehungskräfte erzeugen einen zusätzlichen Binnendruck pB. Dieser Binnendruck erhöht den bei der Idealgasgleichung betrachteten Außendruck p, oder anders ausgedrückt, der Druck auf die Wand wird durch den anziehenden Binnendruck reduziert. Damit kann man den Gesamtdruck p' angeben als
Das Diagramm, in dem die potentielle Energie eines Moleküls in Abhängigkeit von der Entfernung zu einem zweiten Molekül aufgetragen ist, zeigt, daß die potentielle Energie in der direkten Nähe eines zweiten sehr groß ist. Die potentielle Energie ist im Bindungszustand an niedrigs-ten, der Abstand der Moleküle im Bindungszustand sei rB. Entfernt sich das Molekül weiter, so wird die Anziehungskraft der Moleküle schnell kleiner und konvergiert schließlich gegen null.
Diese Anziehungskräfte erzeugen einen zusätzlichen Binnendruck pB. Dieser Binnendruck erhöht den bei der Idealgasgleichung betrachteten Außendruck p, oder anders ausgedrückt, der Druck auf die Wand wird durch den anziehenden Binnendruck reduziert. Damit kann man den Gesamtdruck p' angeben als
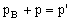
.
 ~ n2
~ n2 ~
~ 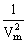
 ~
~ 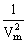
Merke: van der Waalssche Zustandsgleichung 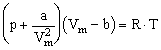 |
Anhand dieser Gleichung können wir nun z.B. die Isothermen realer Gase bestimmen. Für ideale Gase hatten wir festgestellt, das bei konstanter Temperatur die Kurven im p/V-Diagramm Hyperbeln sind. Die Gleichung für reale Gase läßt bereits vermuten, daß diese Kurven für reale Gase komplizierter sind. Um sie zu ermitteln multiplizieren wir zunächst die van der Waals Gleichung aus:
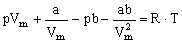 Û
Û 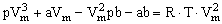
Û 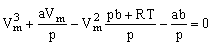
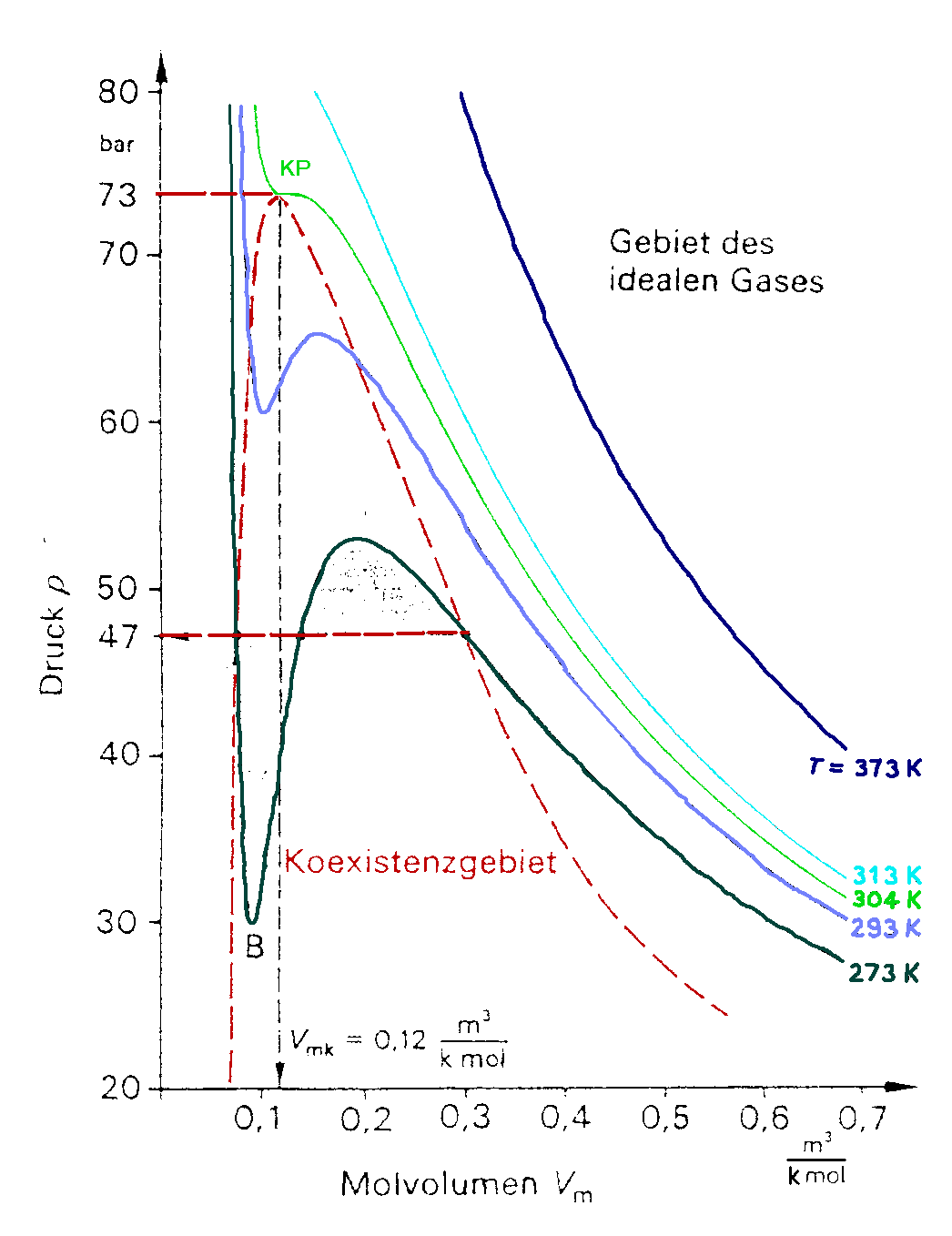
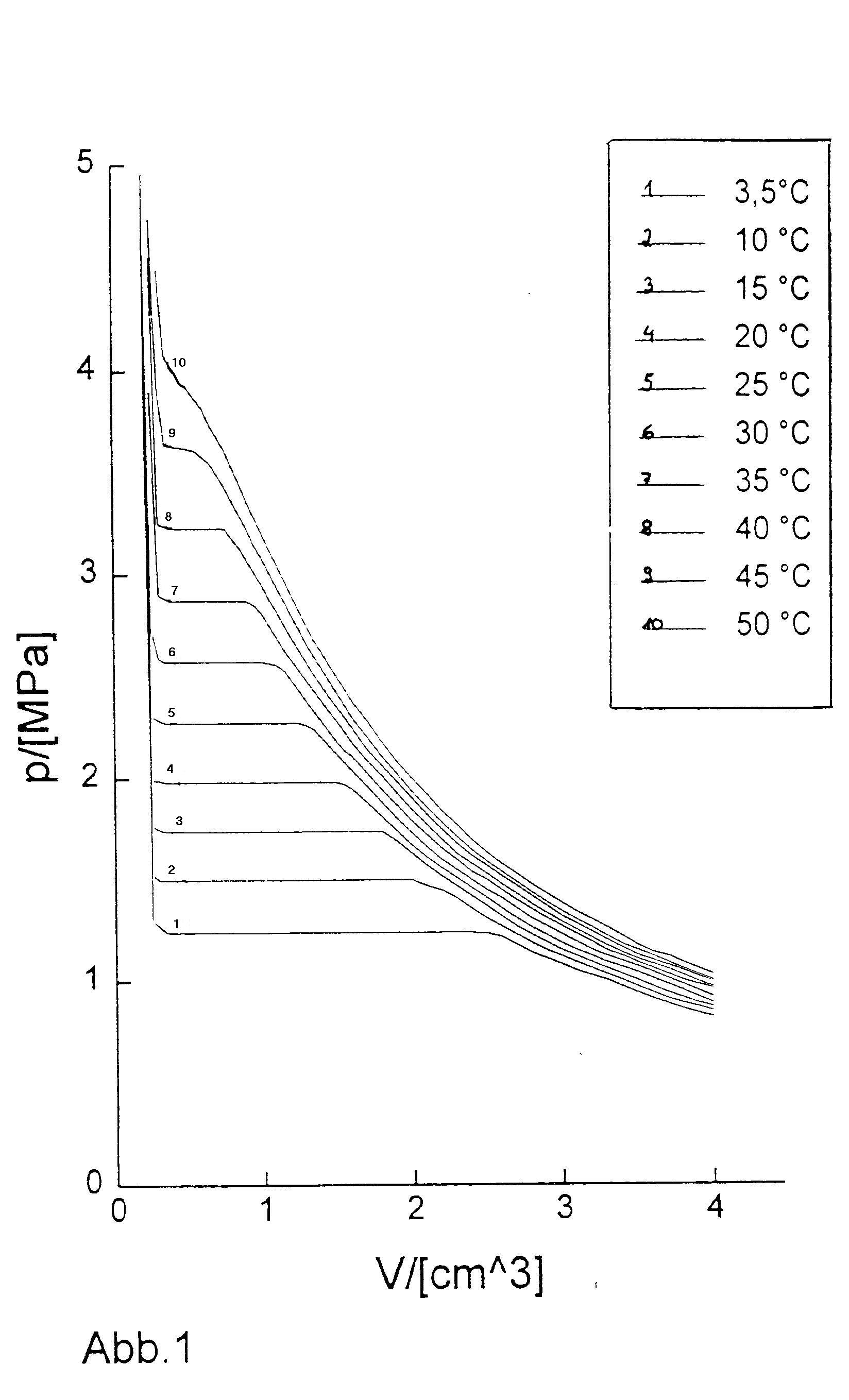
Für eine feste Temperatur T und festen Druck p ergibt sich eine Gleichung dritten Grades für V. Alle Punkte mit derselben Temperatur liegen auf dieser Kurve, sie schneidet die Grade p = const. in drei Punkten. In Abbildung XII.3 sind die Isothermen verschiedener Temperaturen für CO2 aufgetragen.
Für hohe Temperaturen T ähneln die Kurven den Hyperbeln des idealen Gases. Das ist einfach zu verstehen, bedenkt man, daß mit steigender Temperatur das reale Gas ein immer größeres Volumen einnimmt und schließlich angenähert ein ideales Gas darstellt.
Betrachten wir diese Iothermen für kleinere T nun systematisch indem wir bei großem Volumen beginnen.
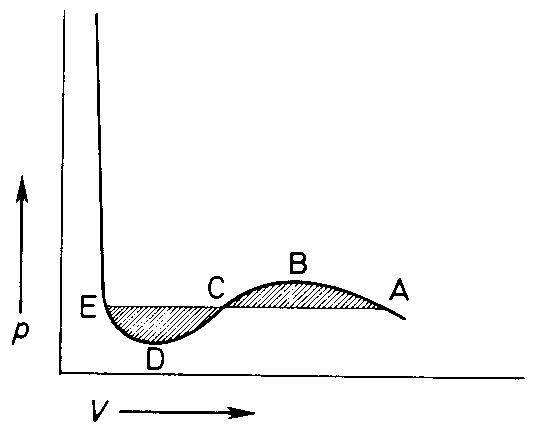
Zunächst steigt mit abnehmendem Vo-lumen der Druck des Gases an, was bei einer Kompression eines Gases ja auch zu erwarten war. Vom Maximum B zum Minimum D der Kurve müßte aber bei abnehmendem Volumen auch der Druck sinken, das entspricht nicht unserer Vorstellung. Bei konstanter Temperatur ist dies nur möglich, wenn die Dichte des Gases sinkt. Das ist tatsächlich der Fall, weil vom Punkt A an das Gas sich teilweise verflüssigt. Während der Verflüssigung bleibt vom Punkt A an der Druck konstant bis Punkt E, an dem das Gas vollständig verflüssigt ist. Die Kurve verläuft also nicht, wie die van der Waalssche Gleichung es angibt, durch ABCDE sondern auf der horizontalen Grade ACD. Diese Korrekturgrade wird Maxwell-Grade genannt. Nachdem sich bei dem zu Punkt E gehörenden Druck das Gas ganz verflüssigt hat, steigt der Druck, den man zur Kompression benötigt, schnell an.
Es zeigt sich, daß weder van der Waals noch Maxwell mit seiner Korrektur der Isotherme die Realität exakt unter jeder Bedingung widergeben. In Wirklichkeit ist es durchaus möglich, kurzzeitig trotz sinkendem Drucks das Volumen einer Flüssigkeit zu vergrößern, d.h. einen Verlauf der Kurve ED teilweise zu messen. Dieses Phänomen wird Siedeverzug genannt. Ab einem gewissen Punkt ist das aber nicht mehr möglich, die Flüssigkeit beginnt zu sieden und die Isotherme springt schlagartig auf die Maxwellgrade zurück. Umgekehrt nennt man das Ausbleiben der Kondensation trotz Reduzierung des Volumens über den Punkt A hinaus Kondensationsverzug.


 Wie ändert sich diese Gleichung unter Berücksichtigung der Ausdehnung von Molekülen und der zwischenmolekularen Kräfte?
Wie ändert sich diese Gleichung unter Berücksichtigung der Ausdehnung von Molekülen und der zwischenmolekularen Kräfte? Ein Molekül mit dem Radius r hat ein Volumen von
Ein Molekül mit dem Radius r hat ein Volumen von
 Das Diagramm, in dem die potentielle Energie eines Moleküls in Abhängigkeit von der Entfernung zu einem zweiten Molekül aufgetragen ist, zeigt, daß die potentielle Energie in der direkten Nähe eines zweiten sehr groß ist. Die potentielle Energie ist im Bindungszustand an niedrigs-ten, der Abstand der Moleküle im Bindungszustand sei rB. Entfernt sich das Molekül weiter, so wird die Anziehungskraft der Moleküle schnell kleiner und konvergiert schließlich gegen null.
Diese Anziehungskräfte erzeugen einen zusätzlichen Binnendruck pB. Dieser Binnendruck erhöht den bei der Idealgasgleichung betrachteten Außendruck p, oder anders ausgedrückt, der Druck auf die Wand wird durch den anziehenden Binnendruck reduziert. Damit kann man den Gesamtdruck p' angeben als
Das Diagramm, in dem die potentielle Energie eines Moleküls in Abhängigkeit von der Entfernung zu einem zweiten Molekül aufgetragen ist, zeigt, daß die potentielle Energie in der direkten Nähe eines zweiten sehr groß ist. Die potentielle Energie ist im Bindungszustand an niedrigs-ten, der Abstand der Moleküle im Bindungszustand sei rB. Entfernt sich das Molekül weiter, so wird die Anziehungskraft der Moleküle schnell kleiner und konvergiert schließlich gegen null.
Diese Anziehungskräfte erzeugen einen zusätzlichen Binnendruck pB. Dieser Binnendruck erhöht den bei der Idealgasgleichung betrachteten Außendruck p, oder anders ausgedrückt, der Druck auf die Wand wird durch den anziehenden Binnendruck reduziert. Damit kann man den Gesamtdruck p' angeben als