 Wärme ist eine Form von Energie.
Wärme ist eine Form von Energie.X.2 Wärme und Wärmemenge
1789 stellte Graf Rumford fest, daß Wärmeentwicklung zum Beispiel durch Reibung bei mechanischer Arbeit entsteht.
Erst um 1850 wurde der eigentliche Charakter von Wärme endgültig erkannt:
 Wärme ist eine Form von Energie.
Wärme ist eine Form von Energie.
Experimentell findet man den Zusammenhang zwischen Temperatur und Wärme: Die Wärme ist proportional zur Temperatur und der Masse des erwärmten Körpers. Das zeigt ein einfaches Gedankenexperiment: Um einen Becher Glas mit einem Kilogramm Wasser mittels eines Tauchsieders mit bekannter Leistung auf eine vorgegebene Temperatur zu erwärmen, braucht man die doppelte Zeit wie zur Erwärmung eines halben Liters Wasser. Darüber hinaus ist die Zeit zur Erwärmung auf eine bestimmte Temperatur der Temperaturerhöhung selbst annähernd proportional.
Aus diesem Gedankenexperiment gewinnt man die Vorstellung, daß der Tauchsieder in einer Zeit eine bestimmte Wärmemenge Q abgibt, die in Wasser zugeführt wird. Zur Erwärmung ist dann eine Wärmemenge erforderlich, die nicht nur die Temperaturerhöhung, sondern auch der Wassermenge proportional ist.
Nach dieser Überlegung müssen wir den in der Mechanik hergeleiteten Begriff der Energie um die Wärmemenge als eine besondere Energieform erweitern. Wärme kann als Energieform weder aus Nichts entstehen noch ohne Ersatz verlorengehen. Die Energieerhaltung besagt, daß sie sich nur in eine andere Energieform, z.B. mechanische Energie, umwandeln kann. Umgekehrt besteht, wie wir wissen, die Möglichkeit, mechanische Energie z.B. durch Reibung in Wärme umzuwandeln.
Die Einheit der Wärmemenge ist entsprechend dieselbe Einheit wie die der Arbeit oder der Energie ganz allgemein:
[Q] = J = Nm
Man definiert eine neue Einheit, die Calorie als:
Definition X.2: Eine Calorie ist die Wärmemenge, die man braucht, um ein Gramm Wasser von 14,5°C aus 15,5°C zu erhitzen. |
Merke: 1 cal = 4,1868 J |
Die Proportionalitätskonstante zwischen Wärmemenge D Q und Temperaturänderung D T einer Masse m wird spezifische Wärme genannt:
Merke: Der Quotient aus Wärmemenge D Q und dem Produkt aus Temperaturänderung D T und der Masse m des erwärmten Körpers wird spezifische Wärme c genannt: |
Die benötige Wärmemenge pro veränderter Temperatur gibt dann das Produkt aus spezifischer Wärme und der Masse des Körpers an. Diese Materialeigenschaft des zu erwärmenden Körpers wird Wärmekapazität genannt.
Merke: Die Wärmekapazität gibt die benötige Wärmemenge pro veränderter Temperatur an: |
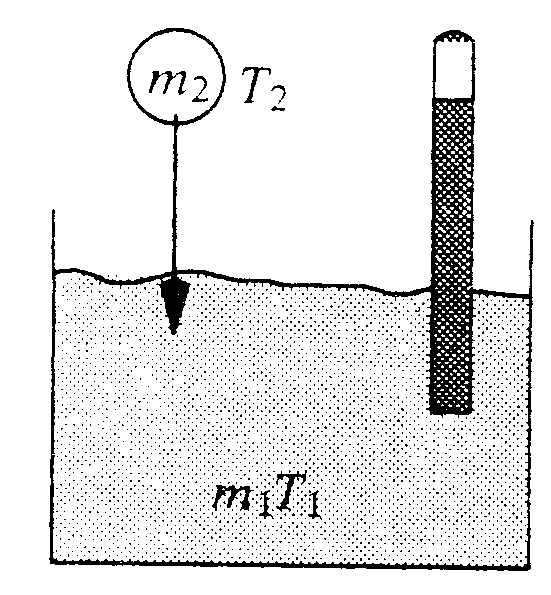
Gedankenexperiment:
Die spezifische Wärmekapazität eines Stoffes kann man am einfachsten mit Hilfe der Mischungsmethode bestimmen. Dazu bringt man einen Körper der Masse m2 und der Temperatur T2 in einen Behälter mit Wasser der Masse m1 und der niedrigeren Temperatur T1. Nach einiger Zeit kann man die Mischtemperatur T des Wassers messen. Aufgrund der Energieerhaltung muß diese vom Metall bei der Abkühlung auf die gemeinsame Temperatur abgegebene Wärmemenge gleich mit der vom Wasser aufgenommenen Wärmemenge sein. Damit gilt die Gleichung:
Û ![]()
Da alle Größen außer c2 meßbar sind und die spezifische Wärme von Wasser laut Definition bekannt ist, kann mit dieser Methode die Wärmekapazität verschiedener Körper gemessen werden.
Die spezifische Wärmekapazität von Wasser ist besonders groß. Deshalb erwärmen sich Meere und Seen sehr viel langsamer als das sie umgebende Land. Dadurch werden die Unterschiede von Land- und Seeklima bedingt.